【题目】下列实验能达到实验目的是

A. 测定空气中氧气含量 B. 探究分子运动 C. 探究燃烧条件 D. 探究铁锈蚀条件
参考答案:
【答案】B
【解析】
A、应该使用足量红磷,确保集气瓶中氧气消耗完,故A错误;
B、本题是探究分子是不断运动的,大烧杯装置外是一个对照实验,氨水能使酚酞试液变红,由于浓氨水易挥发,所以以大烧杯内酚酞试液变为红色,说明的氨气分子通过运动扩散到了整个烧杯中,所以可以达到实验目的,故B正确;
C、燃烧的条件为:必须是可燃物、和氧气接触、达到着火点,正确的实验操作应该是确定一个条件,改变另一个条件来验证燃烧的条件,故C错误;
D、通过对比思想探究铁锈蚀的条件:和水、氧气接触;该实验缺少将干燥的铁钉放到干燥的试管内,用橡皮塞塞上试管口,验证没有水是否能生锈,故D错误。
故选B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
(实验目的)测定金属铁、铜和镁的活动性强弱。
(实验过程)
步骤Ⅰ 将铁片、铜片、镁片分别在空气中加热片刻,观察燃烧现象;
步骤Ⅱ 将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的稀硫酸的试管中;
步骤Ⅲ 将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的硝酸银溶液的试管中。
(实验记录)用“×”表示实验无明显现象,用“√”表示实验有明显现象,(见表);
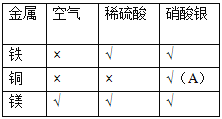
记录表A处应填写的现象是(1)________________,
该反应的化学方程式为(2)______________________。
(实验结论)由步骤Ⅰ和Ⅱ可判断金属铁、铜和镁的活动性由强到弱的顺序是(3)______________________;
(反思交流)小欣同学认为除了以上实验方案以外,在老师提供的药品中(金属已打磨):铁片、铜片、镁片、FeCl2溶液、CuCl2溶液、MgCl2溶液,只选三种药品也能达到实验目的,她选用的药品是(4)__________________________。(任写一种组合即可)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学在探究生铁中铁的含量时,取11.5g生铁样品放入烧杯中,向其中加入100g足量的一定浓度的稀硫酸溶液(杂质不溶于稀硫酸也不与稀硫酸反应),充分反应后烧杯中剩余物质的总质量为111.1g,请回答下列问题:(反应化学方程式为Fe + H2SO4 = FeSO4 + H2↑)
(1)反应生成的氢气的质量为___________克。
(2)该生铁样品中铁的质量分数为多少_______?(精确到0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
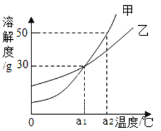
A. 甲和乙的溶解度相等且均为30g
B. 甲物质的溶解度随温度的升高而减小
C. a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
D. 将a2℃150g甲的饱和溶液降温到t1℃,有20g固体析出
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)请用化学符号填空:
①缺_____有可能导致骨骼疏松,②氦气________,③铵根___________,
④写出硫酸铁的化学式并标出铁元素的化合价____________。
(2)在实验室配制50g 15%氯化钠溶液后,请回答下列问题:
①配制过程的步骤是:______、称取氯化钠、量取水、溶解、转移。
②用已调节平衡的托盘天平称取氯化钠时,发现指针偏左,接下来的操作是_____。
A.添加氯化钠 B.减少氯化钠 C.调节平衡螺母 D.添加砝码
③在量取水的体积时,若俯视读数,则会导致氯化钠溶液的溶质质量分数____ (填“<”或“>”)15%。
④在溶解过程中,用玻璃棒搅拌的作用是____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上以石灰石和赤铁矿为主要原料可以制取B和G ,其转化关系如下图所示,已知D、G为单质,C和E的组成元素相同。试回答下列问题:
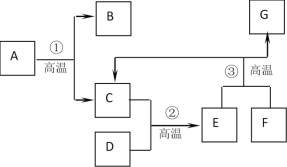
(1)写出两种物质的化学式:B_____,G________。
(2)写出下列反应的化学方程式:反应②:_____,反应③:______,检验气体C:___。
(3)C和E的组成元素相同,但化学性质不同,原因是_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)某同学用市售浓盐酸 (溶质质量分数为37%,密度为1.18gmL-1)配制100g溶质质量分数为10%的稀盐酸。通过计算可知需要浓盐酸_____mL,水 (密度为1gmL-1)_____mL。 (上述两空答案都精确到0.1mL)
(2)某混合物中含有碳酸钙和氯化钙,取该混合物12g,向其中加入一定质量的质量分数为10%的稀盐酸,恰好完全反应,产生4.4g气体。 (假设气体全部逸出)计算:
①所取混合物中碳酸钙的质量_____。
②所加稀盐酸的质量_____。
③反应后所得溶液的溶质质量分数________。 (计算结果精确到0.1%)
相关试题

