【题目】某化学学习小组用如图装置来探究“影响H2O2分解速率”的因素。
(1)写出实验室用二氧化锰催化双氧水分解的化学方程式________________。
【提出问题】影响双氧水分解速率的因素有哪些?
【猜想与假设】a.与双氧水浓度有关;b.与反应时温度有关。
【设计实验】
甲组同学有如下实验设计方案,见表(测量各生成一瓶相同体积O2所需要的时间)。
实验编号 | 温度 | 催化剂 | 浓度 | 时间 |
甲组实验Ⅰ | 25 ℃ | 1 g二氧化锰 | 10 mL 2%H2O2 | 115 s |
甲组实验Ⅱ | 25 ℃ | 1 g二氧化锰 | 10 mL 5%H2O2 | 35 s |
甲组实验Ⅲ | 35 ℃ | 1 g二氧化锰 | 10 mL 5%H2O2 | 15 s |
此实验中宜采用的气体收集方法是:________。
【收集证据】(2)要比较温度对双氧水分解快慢的影响,应选择的实验编号是________。
【得出结论】(3)根据上述实验得出的结论是________________________________________。
【继续探究】H2O2分解生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。写出假设和实验方案。假设:________________________________________________;实验方案:___________________________________________。

(4)乙组同学研究酸、碱对H2O2分解速率的影响的变化曲线如图,请你观察右图回答问题。
①写出一条规律性结论:________________________________________________________;
②乙组提出可以用BaO2固体与硫酸溶液反应制H2O2(已知还生成另一种物质),其化学反应方程式为________________________________;支持这一方案的理由是________________________________。
参考答案:
【答案】 2H2O2![]() 2H2O+O2↑ 排水法 Ⅱ、Ⅲ 温度越高或反应物浓度越大,反应速率越快 双氧水分解生成氧气的快慢还与催化剂的多少有关 取等浓度等体积的双氧水两份,其中一份加入1 g二氧化锰,另一份加入1.5 g二氧化锰,在相同的温度下,比较收集等体积氧气需要的时间长短 相同条件下,H2O2在碱性环境下放出气体速率较快 BaO2+H2SO4===BaSO4↓+H2O2 过氧化氢在酸性环境下分解较慢
2H2O+O2↑ 排水法 Ⅱ、Ⅲ 温度越高或反应物浓度越大,反应速率越快 双氧水分解生成氧气的快慢还与催化剂的多少有关 取等浓度等体积的双氧水两份,其中一份加入1 g二氧化锰,另一份加入1.5 g二氧化锰,在相同的温度下,比较收集等体积氧气需要的时间长短 相同条件下,H2O2在碱性环境下放出气体速率较快 BaO2+H2SO4===BaSO4↓+H2O2 过氧化氢在酸性环境下分解较慢
【解析】分析:(1)从实验室用二氧化锰催化双氧水分解制取和收集较纯净的氧气进行分析;
【收集证据】(2)和【得出结论】(3)从温度对双氧水分解快慢的影响进行分析;
【继续探究】从双氧水分解生成氧气的快慢还与催化剂的多少有关进行分析;
(4)①结合图形进行分析;②![]() 固体与硫酸反应的化学方程式进行分析;
固体与硫酸反应的化学方程式进行分析;
解答: (1) ![]() 在
在![]() 催化下分解前后其质量和性质都没有发生变化,
催化下分解前后其质量和性质都没有发生变化,![]() 在
在![]() 催化下分解生成水和氧气,反应的化学反应为:
催化下分解生成水和氧气,反应的化学反应为: ![]() ;解制取和收集较纯净的氧气,应采用排水集气法进行收集;
;解制取和收集较纯净的氧气,应采用排水集气法进行收集;
(2)要比较温度对双氧水分解快慢的影响,温度应该不同,所以选择的实验编号是Ⅱ、Ⅲ;
(3)假设双氧水分解生成氧气的快慢还与催化剂的多少有关,试验方案为:取等浓度等体积的双氧水两份,其中一份加入1 g二氧化锰,另一份加入1.5 g二氧化锰,在相同的温度下,比较收集等体积氧气需要的时间长短;
(4)①有图可知,相同条件下,H2O2在碱性环境下放出气体速率较快;
②过氧化氢在酸性环境下分解较慢,化学反应方程![]() 。
。
本题答案:(1). ![]() ,排水法 (2). Ⅱ、Ⅲ (3). 温度越高或反应物浓度越大,反应速率越快;双氧水分解生成氧气的快慢还与催化剂的多少有关 ;取等浓度等体积的双氧水两份,其中一份加入1 g二氧化锰,另一份加入1.5 g二氧化锰,在相同的温度下,比较收集等体积氧气需要的时间长短 (4). ①相同条件下,H2O2在碱性环境下放出气体速率较快; ②.
,排水法 (2). Ⅱ、Ⅲ (3). 温度越高或反应物浓度越大,反应速率越快;双氧水分解生成氧气的快慢还与催化剂的多少有关 ;取等浓度等体积的双氧水两份,其中一份加入1 g二氧化锰,另一份加入1.5 g二氧化锰,在相同的温度下,比较收集等体积氧气需要的时间长短 (4). ①相同条件下,H2O2在碱性环境下放出气体速率较快; ②. ![]() , 过氧化氢在酸性环境下分解较慢。
, 过氧化氢在酸性环境下分解较慢。
-
科目: 来源: 题型:
查看答案和解析>>【题目】二氧化碳是一种常见的气体。在实验室里,小明用以下装置制取并检验二氧化碳。

(1)请你写出实验室制取二氧化碳的化学方程式:_____________________________________。
(2)图中仪器a的名称是________。
(3)A装置应当选择右图中的________(填“Ⅰ”或“Ⅱ”),其作用是___________________。
(4)小明发现通入气体后石灰水没有变浑浊,原因可能是_____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验项目所选择的仪器错误的是( )
A. 吸取和滴加少量液体——胶头滴管 B. 取用大块固体药品——药匙
C. 将少量试剂混合进行反应——试管 D. 称量固体药品——天平
-
科目: 来源: 题型:
查看答案和解析>>【题目】衣架是生活中必备的用具,下图是三种不同材质的衣架:
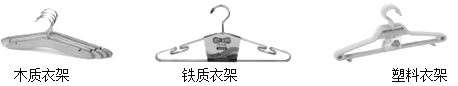
(1)所标物质中属于金属单质的是________(写符号),属于有机合成材料的是________(写名称)。
(2)铁质衣架使用一段时间后会生锈,铁锈主要成分的化学式为________________________;写出用稀盐酸除去铁锈的化学方程式________________________________。
(3)塑料衣架在生活中有着广泛的应用,给我们生活带来了方便但废弃塑料会造成“白色污染”,解决这个问题可以采取的措施是________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度对稀盐酸与氢氧化钠溶液的反应进行了探究,请你参与并填写以下空白。
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应。
第一组同学设计了实验方案一:
实验步骤
实验现象
结论
先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液,并不断振荡,同时测定混合液的pH
pH逐渐________(填“变大”或“变小”),最后pH≥7
稀盐酸与氢氧化钠溶液发生了反应
①请你分析:上述方案中为什么强调只有测得的pH≥7才能证明反应了?_____________________________________________。
②写出稀盐酸与氢氧化钠溶液反应的化学方程式________________________________。
(2)第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后,为探究稀盐酸与氢氧化钠溶液是否恰好完全反应,设计了实验方案二:
实验步骤
实验现象
结论
取少量上述反应后的溶液于试管中,滴加酚酞溶液
若______________
氢氧化钠溶液过量
若无明显现象
稀盐酸与氢氧化钠溶液恰好完全反应
此时有同学提出方案二不能证明稀盐酸与氢氧化钠溶液恰好完全反应,其原因是________________________________,为此,还需要选择________________或________,再进行实验即可。
-
科目: 来源: 题型:
查看答案和解析>>【题目】将铁粉和铜粉混合物10.0 g投入盛100.0 g稀盐酸(足量)的烧杯中,充分反应后,称得剩余物质的总质量为109.8 g,求:
(1)生成氢气的质量是多少克;
(2)该混合物中铜粉的质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲乙丙有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物质按照甲乙丙的顺序不符合要求的是

A.C、CO2、CO
B.H2O2、O2、H2O
C.CuO、Cu、Cu(NO3)2
D.NaOH、NaCl、NaNO3
相关试题

