【题目】(6分)小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装罝如图所示。
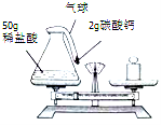
(1)根据实验目的,小明应该测量的数据是_____________(填“只有反应前”“只有反应后”“反应前、后”)整个反应装罝(包括锥形瓶、气球和药品)的质量。
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是_____________,发生反应的化学方程式是__________________________。
③当反应结束时,气球已经完全鼓起,小明发现天平的指针巳经向右偏了。小明又重新称量,记录了数据。他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?你认为出现该实验现象的合理解释最应该是下列各项中的_____________(填序号)。
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律
参考答案:
【答案】(1)反应前、后 (2)②有气泡产生 CaCO3+2HCl═CaCl2+H2O+CO2↑ ③C
【解析】
试题分析:(1)因为要证明质量守恒定律,故小明应该测量的数据是反应前、后整个反应装罝(包括锥形瓶、气球和药品)的质量,从而比较反应前后的总质量的变化情况
(2)②将碳酸钙粉末全部倒入锥形瓶中,碳酸钙能与稀盐酸发生反应:CaCO3+2HCl═CaCl2+H2O+CO2↑,由于发生生成气体二氧化碳,故观察到锥形瓶中液体里出现的现象之一是:有气泡产生
③A、质量守恒定律告诉我们:反应前后原子的种类、数目都不变,错误,B、质量守恒定律告诉我们:反应生成物的总质量等于反应物的总质量,错误,C、由于反应生成气体,使得气球膨胀,这样就收到空气的浮力作用,从而干扰了实验结果,正确,D.生成气体的反应同样遵守质量守恒定律,只是要得到正确的实验结论,应在密闭容器中进行实验,错误,故选C
-
科目: 来源: 题型:
查看答案和解析>>【题目】配制50g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )
A.蒸发皿
B.玻璃棒
C.烧杯
D.量筒
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣小组的同学取10 g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7 g时,恰好完全反应,生成气体的质量与反应时间的关系如下图所示,试回答下列问题:

(提示:Zn+H2SO4=ZnSO4+H2↑)
(1)从图中可以看出,完全反应后生成氢气的质量为 g。
(2)样品中锌的质量为 g。
(3)反应后,所得溶液中硫酸锌的质量分数为多少?
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像能正确反映其对应关系的是
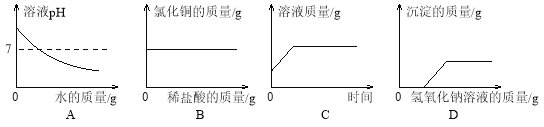
A.向氢氧化钠溶液中不断加水,溶液pH与加入水的质量的关系
B.向盛有氧化铜的烧杯中加入稀盐酸至过量,生成氯化铜质量与加入稀盐酸质量的关系
C.向一定量的饱和硝酸钾溶液中加入硝酸钾固体,溶液的质量与反应时间的关系
D.向盐酸和硝酸铜的混合溶液中滴加氢氧化钠溶液,生成沉淀与加入氢氧化钠溶液的质量关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列措施有利于防止铁制品锈蚀的是
A.自行车链条上的铁锈不及时除去
B.切过咸菜的菜刀不及时清洗
C.工地上的钢管堆放在潮湿的地方
D.家用剪刀不用时,涂上油并放在干燥处
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)微粒观是化学基本观念的重要组成部分,也是化学基本观念中最基础的部分,从微观视角认识和考察物质世界是学习化学应掌握的重要思维方法。
(1)请从“构成物质微粒”的角度对下列物质进行分类:氢气、水、硫酸、铜、氯化钠、氦气。
①由原子构成的物质: ;(写化学式,下同)
②由分子构成的物质: ;
③由离子构成的物质: 。
(2)从宏观和微观的角度将有关物质组成的下列图示补充完整:

-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙两种固体物质的溶解度曲线图。下列说法中不正确的是
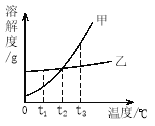
A.t2℃时,甲、乙两种物质溶液的溶质质量分数一定相等
B.t3℃时,将甲、乙的饱和溶液都蒸发掉10g水,析出甲的晶体质量比析出乙的晶体质量大
C.t1℃时,把甲的不饱和溶液变为饱和溶液,溶剂质量不一定变
D.若甲中混有少量乙,可采用降温结晶的方法提纯甲
相关试题

