【题目】下列图象能正确反应对应变化关系的是()
A. 将水电解一段时间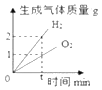
B. 向等质量镁、铝中分别加入稀盐酸至过量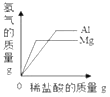
C. 向盛有一定质量硝酸铜、硝酸银的混合溶液中加入铁粉至过量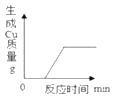
D. 向一定量铁粉中逐滴加入稀盐酸至过量
参考答案:
【答案】C
【解析】
A、通电分解水,生成氢气和氧气的体积(而不是质量)之比为2:1,故图象不能正确反应对应变化关系。
B、等质量镁、铝分别和足量稀盐酸反应,若消耗盐酸相同,则生成氢气质量相同,故开始两斜线重合,后因盐酸过量,铝消耗盐酸多,生成氢气多,拐点高些,故图象不能正确反应对应变化关系。
C、铁的金属活动性比铜、银强,向盛有一定质量硝酸铜、硝酸银的混合溶液中加入铁粉至过量,铁先与AgNO3溶液反应生成硝酸亚铁溶液和银,再与硝酸铜溶液反应生成硝酸亚铁溶液和铜,故图象能正确反应对应变化关系。
D、铁与稀盐酸反应生成氯化亚铁溶液和氢气,溶液质量增加,当铁反应完后继续加稀盐酸,稀盐酸也是一种溶液,故溶液质量仍会增加,图象不能正确反应对应变化关系。
故选:C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙、丁是常见的化合物,它们有如下图所示转化关系(部分物质已略去)。甲是相对分子质量为16的气体;乙是最常见的液体;丁是白色难溶固体,其中金属元素的质量分数为40%。
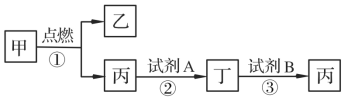
(1)则甲的化学式为_____。(2)写出①②反应的化学方程式_____,_____
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图所示的实验装置图回答:

(1)写出编号的仪器名称:①_____;②_____;
(2)实验室常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为:_____;制取并收集CO2,应选用的装置为_____(填序号)。
(3)如果要检验二氧化碳是否收集满,可将_____。
(4)如图所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是:_____,植物油上方原有空气对实验结果_____(填“有”或“无”)明显影响.
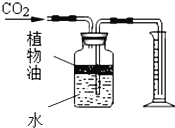
(5)在加热氯酸钾和二氧化锰混合物制氧气实验中,混合物总质量100g,反应一段时间后,二氧化锰的质量分数由20%变为25%求氯酸钾的分解率。_____。(提示:分解率是分解的质量比原质量)
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属元素锂被誉为“能源元素”,锂及锂的化合物具有优异性能,广泛应用于电子、宇 航、核能等领域,中国科学院某研究小组设计一种高性能锂空气电池,其反应原理为:2Li+O2
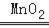 Li2O2.已知锂原子结构示意图为
Li2O2.已知锂原子结构示意图为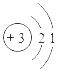 ,下列有关说法错误的是()
,下列有关说法错误的是()A. MnO2在该反应中起催化剂作用
B. 锂元素化学性质与钠元素相似
C. Li2O2中氧元素化合价为﹣2
D. 该反应是化合反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】小金为探究铁制品锈蚀的条件,进行如下实验:
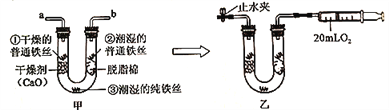
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象
现象
①干燥的普通铁丝
没有明显变化
②潮湿的普通铁丝
较多红褐色锈斑
③潮湿的纯铁丝
没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是_______。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是_____。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)建造航母用到了钛合金。构成金属钛的粒子是___(填“原子”分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO4
 4HF+2X+TiO2,X的化学式为___。
4HF+2X+TiO2,X的化学式为___。(2)航母外壳用涂料覆盖,是为了防止钢铁材料与___接触而锈蚀。
(3)铝热剂是航母制造时常用焊接材料,其反应原理是铝在高温条件下与氧化铁反应得到熔融的铁与另一种氧化物,该反应化学方程式为___,该反应基本反应类型是___。
(4)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验,其中能达到目的是___(填序号)。
A 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C ZnCl2溶液中加入足量铁粉后,再加入Cu粉
-
科目: 来源: 题型:
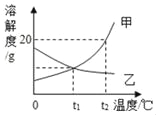
查看答案和解析>>【题目】如图是甲、乙两种固体物质的溶解度曲线,请回答:
(1)在___时,甲、乙两种物质的溶解度相同。
(2)不改变溶剂的质量,将t1℃甲的饱和溶液变为不饱和溶液可 采用方法是___。
(3)t2℃时,将25g甲放入装有100g水中,充分搅拌发现固体先全部溶解,一段时间后又有晶体析出,请解释甲固体全部溶解的原因___。
(4)下列有关说法正确的是___(填序号)。
①甲中含有少量的乙可采用降温结晶的方法提纯甲
②t2℃时,甲溶液的溶质质量分数比乙溶液溶质质量分数大
③t2℃时,将等质量甲、乙分别加水配成饱和溶液,所得甲溶液质量比乙溶液小
④将t2℃时甲、乙饱和溶液降温至t1℃时,所得甲、乙溶液的溶质质量分数相等
⑤将t2℃时120g甲的饱和溶液降温至t1℃时,可析出20g甲晶体
相关试题

