【题目】物质甲和乙的转化关系如图所示(“→”表示一步进行的反应)。
![]()
(1)若甲乙都是单质,甲是铁。
转化l反应的化学方程式为___________(写一个)。
转化Ⅱ为高温下,乙与氧化铁反应生成甲和水,该反应属于___________(填基本反应类型)。
(2)若甲、乙为元素种类相同的氧化物
①甲中含碳元素的质量分数高于乙转化Ⅱ的化学方程式为___________。
②若转化l发生的反应是CaO2+2H2O=X+Ca(OH)2,X为物质乙,乙的名称为___________。转化Ⅱ的化学方程式为___________。
参考答案:
【答案】 Fe+2HCl=FeCl2+H2↑ 置换反应 CO2 + C ![]() 2CO 过氧化氢 2H2O2
2CO 过氧化氢 2H2O2 ![]() 2H2O + O2↑
2H2O + O2↑
【解析】本题是框图式推断题,首先根据题中提供的信息和题中的转化关系推导出另一种物质,最后将推出的物质代入转化关系中进行验证。
(1)若甲乙都是单质,甲是铁,则乙可能中氢气,代入示意图,假设成立。转化l反应可以用铁与稀盐酸反应生成氯化亚铁和氢气,化学方程式为Fe+2HCl=FeCl2+H2↑;转化Ⅱ为高温下,氢气与氧化铁反应生成铁和水,该反应是一种单质与一种化合物反应生成另一种单质和另一种化合物,属于置换反应;
(2)若甲、乙为元素种类相同的氧化物,可能是一氧化碳或二氧化碳,代入示意图,假设成立。
①一氧化碳中含碳元素的质量分数高于二氧化碳,转化Ⅱ反应是二氧化碳在高温下与碳反应生成一氧化碳,化学方程式为CO2 + C ![]() 2CO;
2CO;
②若转化l发生的反应是CaO2+2H2O=X+Ca(OH)2,根据质量守恒定律,反应前后原子种类和数目保持不变,X化学式为H2O2,名称为过氧化氢。转化Ⅱ反应是过氧化氢在二氧化锰催化下转化为水和氧气,化学方程式为2H2O2 ![]() 2H2O + O2↑。
2H2O + O2↑。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行了探究。

【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是_______________________________________。
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是_______________。
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验________________(填“能”或“不能”)验证猜想(二)的正确性,原因是_______________。
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应的化学方程式为________________________________________。
(3)若验证猜想(四)是否正确,下列试剂中可选用的有_____________(填序号)。
①氢氧化钠溶液 ②氯化钙溶液
③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行________________操作即可从废液中得到NaCl固体。此方法的缺点是__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。

(1)写出图中仪器a名称______________;
(2)实验室制取二氧化碳的化学方程式是________________,应选择的气体发生装置是__________(填序号);
(3)实验室用A装置制取氧气的化学方程式是________________,该反应为__________反应(填反应类型),若用盛满水的F装置收集氧气,应从导管________(填①或②)通入;
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,常温下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水;那么在制取和收集氨气时,应该从图中选择的发生装置是_________,收集装置是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】图为元素周期表中部分元素的相关信息。
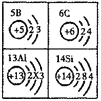
(1)原子序数为13的元素,x=___________。在化学变化中,该原子易___________(填“得”或“失”)电子形成离子,其离子符号是___________。
(2)硼(B)属于___________(填“金属”或“非金属”)元素。其化学性质与铝元素相似的原因是___________。
(3)碳酸中碳元素与硅酸中硅元素在周期表中属于同一纵行。两元素的最高正价相同,则硅酸的化学式为___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟
加入稀硫酸后20分钟
加入稀硫酸后
加入稀硫酸后40分钟
加入稀硫酸后50分钟
232.4g
232.3g
232.2g
232.1g
232.1g
(1)完全反应后生成氢气的质量为______g.
(2)计算该黄铜中铜的质量分数为________(写出计算过程).
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定某铜锌合金中锌的含量,取50g样品进行实验,将l00g稀盐酸分五次加入该样品中(杂质不溶于水也不参与反应,反应原理为:Zn+2HCl=ZnCl2+H2↑),充分反应后测得生成气体的总质量如表所示:
加入稀盐酸的质量/g
20
20
20
20
20
生成气体的总质量/g
0.05
0.10
m
0.20
0.20
试求:(1)m的数值为___________。
(2)该铜锌合金中锌的质量分数是___________?(写出计算过程)
-
科目: 来源: 题型:
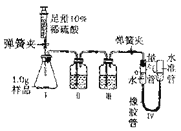
查看答案和解析>>【题目】某过碳酸钠样品中含有少量的碳酸钠等杂质,为测定其纯度,某化学小组同学利用如图装置展开如下探究:
[资料在线]
①过碳酸钠(Na2CO4)和稀硫酸反应的原理为:
2 Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O
②碳酸钠与稀硫酸反应后生成硫酸钠、二氧化碳和水。
③浓硫酸具有强吸水性。氢氧化钠溶液能吸收二氧化碳。
④含钠的化合物可溶于水,样品中其它杂质不溶于水且不参与反应。
⑤该实验条件下,氧气的密度为l.43g/L、二氧化碳的密度l.97g/L。
[实验步骤]
a.连接仪器并检查装置气密性。
b.向装置Ⅰ中的锥形瓶加入1.0g样品,由注射器缓缓注入稀硫酸,待到完全反应后,利用装置Ⅳ测得反应生成的气体体积为82.6 mL;装置I中的溶液经处理,称得硫酸钠固体质量为1.1g。
c.根据测得数据,计算样品中过碳酸钠的质量分数。
[回答问题]
(1)判断样品与稀硫酸完全反应的现象是___________。
写出碳酸钠与稀硫酸反应的化学方程式:___________。
(2)装置Ⅱ和Ⅲ的广口瓶中盛有足量的药品是___________(填标号)。
A.Ⅱ—浓硫酸、Ⅲ—氢氧化钠溶液 B.Ⅱ—氢氧化钠溶液、Ⅲ—浓硫酸
(3)甲同学通过称量装置I中实验前后固体的质量、乙同学通过读取装置IV中气体的体积,分别计算出样品中过碳酸钠质量分数。
①乙同学计算过程中,需要选用___________ (填“氧气”或“二氧化碳”)的密度。
②两位同学的实验结果不同,经分析乙同学实验方案正确。甲同学的实验方案不准确的原因是___________。
相关试题

