【题目】如图所示,进行中和反应实验:

(1)在A的实验中,滴入酚酞试液后,溶液由无色变为______色。
(2)写出C的溶液中溶质可能存在的几组情况(用化学式表示)_____________________________
(3)使10 ml氢氧化钠恰好中和,需滴加溶有0.01mol氯化氢的稀盐酸溶液,
①0.01mol氯化氢分子个数为____________________________个;
②与含有0.01mol氯化氢的稀盐酸完全中和需要的氢氧化钠的物质的量为多少_____________?(列式计算)
参考答案:
【答案】 红 NaCl 或NaCl和HCl 6.02 1021 NaOH+ HCl ==NaCl+H2O
11
x0.01mol
1/x=1/0.01molx=0.01mol
【解析】(1)氢氧化钠溶液呈碱性,滴入酚酞试液后,使无色酚酞变为红色。(2)氢氧化钠与盐酸反应的方程式为:NaOH+ HCl ==NaCl2 +H2O。所以当反应后的溶液中一定有生成物,还可能有过量的反应物。C的溶液中溶质可能存在的几组情况①NaCl (刚好完全反应)②NaCl和HCl(盐酸过量)③NaCl和NaOH(NaOH过量)
(3)①由每1摩尔任何物质含有阿伏伽德罗常数(约6.02×1023)个微粒;所以0.01mol氯化氢分子个数为6.02 1021,②与含有0.01mol氯化氢的稀盐酸完全中和需要的氢氧化钠的物质的量为x,NaOH+ HCl ==NaCl2 +H2O
1 1
x 0.01mol
1/x=1/0.01mol x=0.01mol ,答:略
-
科目: 来源: 题型:
查看答案和解析>>【题目】氧气的下列性质中,有一项与其它三项有着本质的区别,它是
A. 无色 B. 无味 C. 难溶于水 D. 能支持燃烧
-
科目: 来源: 题型:
查看答案和解析>>【题目】为验证“酸的化学性质”,某班同学在实验室进行如图实验.请分析并回答相关问题:
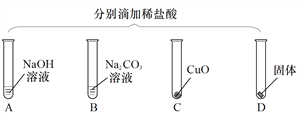
①B试管中的现象是___________,
②C中发生反应的现象是______________________________,
反应的化学方程式 _____________________________________ 。
③要全面验证酸的化学通性,D试管中能与酸反应的固体单质是______(写一种即可)。
④实验完成后,将全部废液倒入废液缸内,测得pH=2,则废液中所含溶质最多有_________种(溶质不计指示剂与气体)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)探究金属性质:
图1是探究金属化学性质,图2是金属化学性质网络图。
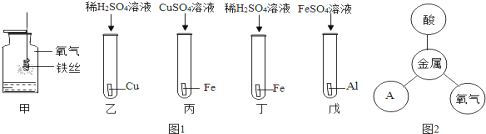
①图1甲中反应现象是________________,其反应的化学方程式为_________________;
②图1只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,
由强到弱的顺序是_____________(填元素符号);依据图1完成金属性质网络,图2中的A属于________(填物质类别);
-
科目: 来源: 题型:
查看答案和解析>>【题目】写出有水生成的反应(每种反应类型写一个方程式)
化合反应:__________________________;分解反应:______________________;
置换反应:__________________________;复分解反应:____________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示的是甲、乙两种固体物质的溶解度曲线, 下列叙述正确的是( )
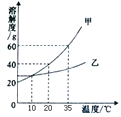
A. 甲的溶解度大于乙的溶解度
B. 曲线乙可以表示氢氧化钙的溶解度曲线
C. 降低温度可使接近饱和的甲溶液变成饱和溶液
D. 35℃时100g甲的溶液中含甲的质量60g
-
科目: 来源: 题型:
查看答案和解析>>【题目】某元素原子得到2个电子后形成具有与Ne
 相同核外电子排布的粒子,下列说法正确的是( )
相同核外电子排布的粒子,下列说法正确的是( )A.该粒子为阳离子
B.该粒子原子序数为10
C.该粒子可表示为O2﹣
D.该元素位于元素周期表第一周期
相关试题

