【题目】柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:

(1)写出反应1的化学方程式 ,该反应属于基本反应类型中的 反应;
(2)操作1的名称为 ;
(3)写出反应2的化学方程式 ;
(4)反应3中会有气体生成,该气体是 ;
(5)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为 。
参考答案:
【答案】
(1)Fe+H2SO4═FeSO4+H2↑ 置换
(2)过滤
(3)FeSO4+Na2CO3═Na2SO4+FeCO3↓
(4)二氧化碳
(5)7:9
【解析】
试题分析:
(1)反应1,即铁与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(2)操作1是将铁粉与溶液分离,操作1的名称为过滤;
(3)反应2,即硫酸亚铁与碳酸钠反应生成碳酸亚铁沉淀和硫酸钠,反应的化学方程式为FeSO4+ Na2CO3═Na2SO4+FeCO3↓;
(4)反应3中会有气体生成,碳酸盐与酸反应生成二氧化碳,则该气体是二氧化碳。
(5)柠檬酸亚铁中铁元素和碳元素质量比为56:(12×6)=7:9。
故答案为:
(1)Fe+H2SO4═FeSO4+H2↑ 置换
(2)过滤
(3)FeSO4+Na2CO3═Na2SO4+FeCO3↓
(4)二氧化碳
(5)7:9
-
科目: 来源: 题型:
查看答案和解析>>【题目】NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是( )

A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
-
科目: 来源: 题型:
查看答案和解析>>【题目】 人体结石有多种,其中一种含有较多的草酸钙(CaC2O4),CaC2O4中碳元素的化合价是
A.+1 B.+2 C.+3 D.+4
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质X的化学式为H2C2O4,可发生如下反应:
aH2C2O4
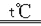 bH2O↑+cCO2↑+dY↑
bH2O↑+cCO2↑+dY↑取90g X,在t℃完全分解,产物通过足量浓硫酸,浓硫酸增重18g,另取90gX,在t℃完全分解,产物通过足量碱石灰(CaO和NaOH的固体混合物),碱石灰增重62g,则下列说法不正确的是(已知气体Y不与浓硫酸或碱石灰发生反应)( )
A.CO2的质量为44g B.气体Y的质量为28g
C.气体Y可能为甲烷 D.方程式中b和c的比为1:1
-
科目: 来源: 题型:
查看答案和解析>>【题目】煤的综合利用有利于保护自然环境和社会的可持续发展。
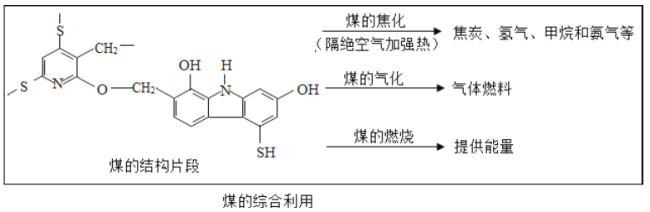
(1)由煤的结构片段可知:煤的组成元素中除C、H、O、S外还含有 (填元素符号)。
(2)煤的焦化属于 变化;焦化获得的焦炭可用于高炉炼铁,高炉内CO和Fe2O3反应的化学方程式为 ;焦化获得的氨气可用于制取氮肥,区分(NH4)2SO4和K2SO4两种化肥可选用的试剂是 (填对应选项的字母)。
A.氯化钡 B.盐酸 C.熟石灰
(3)煤的气化过程中主要反应是碳与水蒸气生成两种气体燃料,其中一种是单质,该单质是 ;
(4)提高煤的燃烧效率能节约煤碳资源,写出一种提高煤的燃烧效率的方法: 。煤中加入适量石灰石燃烧,可发生反应:2CaCO3+O2+2SO2
 2CaSO4+2CO2,煤中加入石灰石对环境的意义是 。
2CaSO4+2CO2,煤中加入石灰石对环境的意义是 。 -
科目: 来源: 题型:
查看答案和解析>>【题目】某学生用量筒量取液体,量筒放平稳且面对刻度线,初次视线与量筒内液体凹液面最低处保持水平,读数为19 mL。倒出部分液体后,俯视凹液面最低处,读数为11 mL,则该学生倒出的液体的体积( )
A.等于8 mL B.小于8 mL C.大于8 mL D.无法判断
-
科目: 来源: 题型:
查看答案和解析>>【题目】从微观的角度了解物质及其变化,有助于更好的认识物质组成和变化的本质。
(1)氟原子的结构示意图为
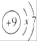 ,则x= ,在化学反应中氟原子易 (填“得到”或“失去“)电子。
,则x= ,在化学反应中氟原子易 (填“得到”或“失去“)电子。(2)铝原子失去3个电子形成离子的离子符号为 。
(3)如图为Mn和CuSO4溶液反应的示意图,回答下列问题:
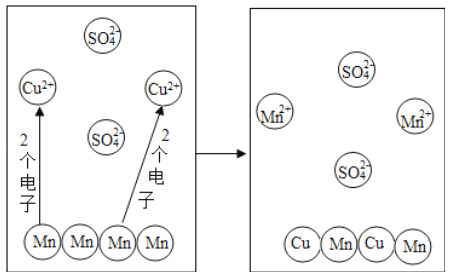
实际与Mn反应的粒子是 ;
反应中失去电子的粒子是 ;
由反应可知金属的活泼性:Mn Cu(填“>”或“<”);
④该反应中化合价没有改变的元素或根是 (填对应选项的字母)。
A.锰元素 B.铜元素 C.硫酸根
相关试题

