【题目】O2、H2、CO2是中学化学中常见的气体,请根据下列装置图回答问题:
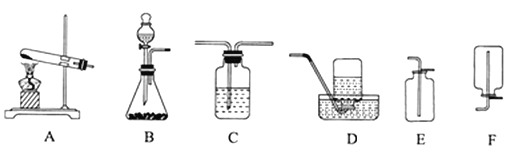
(1)实验室制取CO2的发生装置应选用_____(用字母A~F填空)装置,其中的玻璃仪器(连接装置除外)的名称是________;
(2)实验室用B装置制取O2时,加入的固体起______作用;该反应的化学方程式为_______。
(3)实验室用C装置干燥H2时加入的试剂是_____(填名称),收集H2选用的装置是D或F,其原因是________。
参考答案:
【答案】 B 分液漏斗、锥形瓶 催化 2H2O2![]() 2H2O+O2↑ 浓硫酸 氢气不溶于水,且密度比空气小
2H2O+O2↑ 浓硫酸 氢气不溶于水,且密度比空气小
【解析】(1)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;其中的玻璃仪器有锥形瓶和分液漏斗; (2)装置B适用于固液常温下制取气体,则为实验室用过氧化氢制氧气,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2MnO22H2O+O2↑;(3)浓硫酸具有吸水性,所以可用盛有浓硫酸的装置C来干燥氢气,氢气的密度比空气小,所以可用向下排空气法收集氢气,氢气难溶于水,所以可用排水法来收集。
-
科目: 来源: 题型:
查看答案和解析>>【题目】室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
⑴由如图可知,盐酸与氢氧化钠溶液中和反应是___________(填“吸热”或“放热”或“无热量变化”)反应。
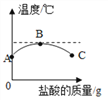
⑵在C处溶液中加入石蕊,溶液呈___________。
⑶B处溶液的溶质是___________(填化学式)。
⑷B到C的过程中溶液的pH逐渐___________(填“增大”或“减小”或“无变化”)。
⑸在A点溶液中加入硫酸铜溶液,现象为____________,化学方程式为____________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】酸、碱、盐溶解性表是学习化学的重要工具。下表列出了“部分酸、碱、盐在20 ℃时的溶解性”,请利用此表完成以下任务:
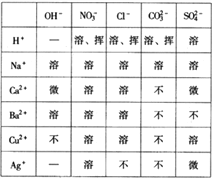
⑴查:Ba(OH)2的溶解性________________。
⑵写化学式:一种酸__________,一种不溶于水的盐___________。
⑶判断:氯化钠溶液与硝酸钙溶液能否发生反应________________,理由是________________。
⑷写化学方程式:氯化钡溶液与表中的一种盐反应______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】3%的硼酸溶液可用于清洗皮肤的小面积创伤。现配制300g质量分数为3%的硼酸溶液,实验操作如下:
⑴称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数。
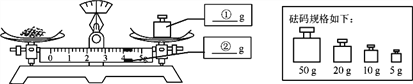 ______________________
______________________⑵量取水的体积:用量筒取_________mL水(密度为1g/cm3)。
⑶溶解:用到的玻璃仪器是__________。
⑷装瓶、贴标签:在下图的标签中填上相应的内容。
 _____________________
_____________________⑸反思:若称取的硼酸中含有杂质,则所配制的溶液的质量分数会______(填“偏大”、“偏小”或“无影响”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】将碳酸钠溶液中滴入氯化钙溶液至恰好完全反应。
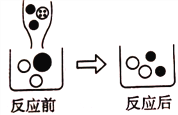
⑴可以观察到的现象是______________。
⑵下图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子(填离子符号):
 _____________
_____________ ______________。
______________。⑶下列物质能与碳酸钠溶液反应产生类似上述实验现象的是______________(双选)。
A.HCl B.Ca(OH)2 C. (NH4)2SO4 D.BaCl2
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了节约林木资源,近几年兴起了一种含碳酸钙的“石头纸”,这种“石头纸”是用沿海水产养殖中大量废弃贝壳制得的。为测定其中碳酸钙(杂质不溶于水也不与水反应)的含量,某校化学兴趣小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取25.0 g样品粉碎放入烧杯中,加入一定质量分数的稀盐酸,所加稀盐酸的质量与生成气体的质量关系如图所示:
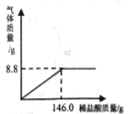
(1)计算“石头纸”中碳酸钙的质量分数。
(2)完全反应后烧杯内溶液的溶质的质量分数是多少?(结果精确到0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】A﹣H都是初中常见的物质,其中D为蓝色沉淀,A、E是组成元素相同的两种气体,B为红色固体,F、H为黑色固体,他们之间转化关系如下图(反应条件及部分反应物和生成物已略去 )。
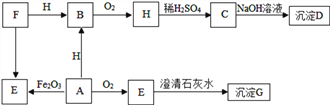
⑴C的化学式是________。
⑵写出反应H→C化学方程式____________________________。
⑶写出反应A→E化学方程式_____________________________写一个)。
⑷答出G的一种用途____________________________________。
相关试题

