【题目】室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
⑴由如图可知,盐酸与氢氧化钠溶液中和反应是___________(填“吸热”或“放热”或“无热量变化”)反应。
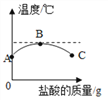
⑵在C处溶液中加入石蕊,溶液呈___________。
⑶B处溶液的溶质是___________(填化学式)。
⑷B到C的过程中溶液的pH逐渐___________(填“增大”或“减小”或“无变化”)。
⑸在A点溶液中加入硫酸铜溶液,现象为____________,化学方程式为____________________。
参考答案:
【答案】 放热 红色 NaCl 减小 蓝色沉淀 CuSO4+2NaOH=== Na2 SO4+Cu(OH)2↓
【解析】(1)由图可知,氢氧化钠与稀盐酸反应是放热反应;
(2)由图可知,c处的稀盐酸过量,故溶液显酸性,故溶液显红色;
(3)b处的氢氧化钠与稀盐酸恰好完全反应,故溶液中的溶质是氯化钠,化学式为NaCl;
(4)B到C处的稀盐酸逐渐过剩,故pH逐渐降低;
(5)A点的溶液显碱性,故加入硫酸铜后生成蓝色的氢氧化铜沉淀;反应方程式为CuSO4+2NaOH=== Na2 SO4+Cu(OH)2↓
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
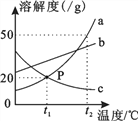
A. t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B. P点表示t1℃时,a、c两种物质的溶解度相等
C. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
D. t1℃时, a、c两种物质的饱和溶液中,溶质质量分数均为20%
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图象不能反映客观事实的是
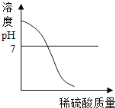
A.往NaOH溶液中逐滴加入稀硫酸
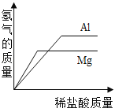
B.往等质量的铝和镁中加入足量的稀盐酸
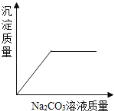
C.往稀盐酸和CaCl2溶液加入Na2CO3溶液
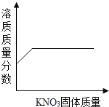
D.等温条件下往接近饱和的硝酸钾溶液中不断加入硝酸钾固体
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
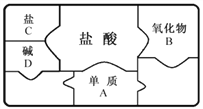
⑴A不可能是______(填标号)。
a.Mg b.Fe c.Ag d.Zn
⑵若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为______________。
⑶若C为碳酸钠。
①C与D的反应属于______(填基本反应类型)。
②将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有______种。
⑷D与盐酸反应的化学方程式为_____________________(写一个)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】酸、碱、盐溶解性表是学习化学的重要工具。下表列出了“部分酸、碱、盐在20 ℃时的溶解性”,请利用此表完成以下任务:
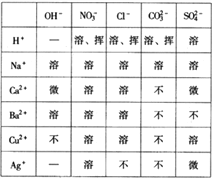
⑴查:Ba(OH)2的溶解性________________。
⑵写化学式:一种酸__________,一种不溶于水的盐___________。
⑶判断:氯化钠溶液与硝酸钙溶液能否发生反应________________,理由是________________。
⑷写化学方程式:氯化钡溶液与表中的一种盐反应______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】3%的硼酸溶液可用于清洗皮肤的小面积创伤。现配制300g质量分数为3%的硼酸溶液,实验操作如下:
⑴称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数。
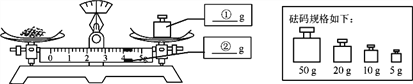 ______________________
______________________⑵量取水的体积:用量筒取_________mL水(密度为1g/cm3)。
⑶溶解:用到的玻璃仪器是__________。
⑷装瓶、贴标签:在下图的标签中填上相应的内容。
 _____________________
_____________________⑸反思:若称取的硼酸中含有杂质,则所配制的溶液的质量分数会______(填“偏大”、“偏小”或“无影响”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】O2、H2、CO2是中学化学中常见的气体,请根据下列装置图回答问题:
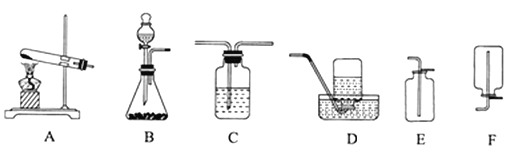
(1)实验室制取CO2的发生装置应选用_____(用字母A~F填空)装置,其中的玻璃仪器(连接装置除外)的名称是________;
(2)实验室用B装置制取O2时,加入的固体起______作用;该反应的化学方程式为_______。
(3)实验室用C装置干燥H2时加入的试剂是_____(填名称),收集H2选用的装置是D或F,其原因是________。
相关试题

