【题目】质量守恒定律是化学反应中的重要规律,我能运用此规律解答下列问题:
(1)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+3O2=2CO2+3H2O(反应条件已略去),则X的化学式为 .
(2)在催化剂并加热的条件下,A与B反应生成C和D.反应前后分子变化的微观示意图所下所示:
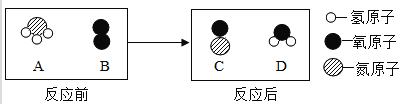
①下列说法正确的是 (填序号).
a.该反应类型为置换反应
b.4种物质中只有D属于氧化物
c.反应前后,氮元素化合价升高
d.化学反应中分子可以再分,而原子不能
②该反应的化学方程式为 .
参考答案:
【答案】(1)C2H4 (2)①abcd ②4NH3+3O2![]() 2N2+6H2O
2N2+6H2O
【解析】
试题分析::(1)根据反应前后原子的种类和数目都不变:X+3O2═2CO2+2H2O,可以知道反应后有2个C,4个H,6个O,而反应前只出现了6个O,故X中含有2个C,4个H,化学式为C2H4.(2)根据质量守恒定律反应前后原子的种类和数量不变,配平方程式,故化学方程式为:4NH3+3O2![]() 2N2+6H2O
2N2+6H2O
a、根据置换反应是指一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,故a正确;
b、根据氧化物是指由两种元素组成,其中一种为氧元素的化合物,可知b正确;
c、反应前,氮元素显﹣3价,反应后,氮元素显0价,故c正确;
d、化学反应中分子可以再分,而原子不能再分正确;故选abcd
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是实验室制取气体时常见的装置(其中G、I为干燥装置),根据装置回答下列问题:
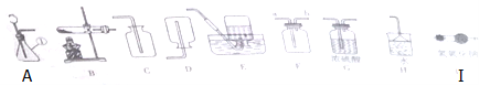
(1)仪器①的名称 .
(2)用A装置制取的某气体可使带火星的木条复燃,请写出用A装置制取该气体的化学方程式 .
(3)现用G装置收集到一瓶无色无味的气体,欲检验其是否为CO2的方法是 ;若改用F装置收集该气体,则气体应从 (填“a”或“b”)通入.
(4)常温下,氨气(NH3)是一种有刺激性气味的气体,极易溶于水,密度比空气小,溶液呈碱性.实验室制取氨气的原理是NH4C1(固)与Ca(OH)2(固)混合共热.现要制得干燥的氨气并处理尾气,防止污染空气,所选择的装置连接顺序依次是B→ →F→H(填装置序号).
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关催化剂的说法正确的是( )
A. 在化学反应后其质量减小 B. 催化剂只能加快化学反应速率
C. 一个反应的催化剂可以有多种 D. 在化学反应后其性质一定不发生改变
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B是金属氧化物,如图所示是各物质之间的相互转化关系.请回答:
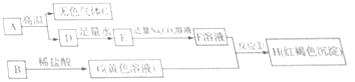
(1)写出下列物质的化学式:B ;D .
(2)反应①的化学方程式为 .
(3)举出E在农业生产中的一种用途 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】元素周期表是化学学习的重要工具,依据下表回答问题:
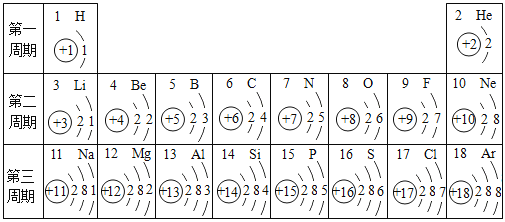
(1)表中12号元素属于 (填“金属”或“非金属”)元素,在化学反应中比较容易 (填“失去”或“得到”)电子,形成 (填离子符号).
(2)由11号元素与16号元素组成的常见化合物的化学式 .
(3)表中同一周期原子的核外电子排布规律是 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学在实验室发现一瓶由碳酸钠和氯化钠组成的混合溶液.为了测定该混合溶液中碳酸钠的质量分数,该同学设计了如下实验:取该混合溶液50g,向其中逐滴加入稀盐酸,当加入盐酸的质量为15g、30g、45g、60g时,生成气体的质量见下表(气体的溶解度忽略不计).
第Ⅰ组
第Ⅱ组
第Ⅲ组
第Ⅳ组
稀盐酸的质量/g
15
30
45
60
生成气体的质量/g
1.8
n
4.4
4.4
(1)第Ⅱ组数据n为 g.
(2)混合溶液中碳酸钠的质量分数是多少?(写出计算过程,结果精确至0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
R
O2
CO2
H2O
反应前质量(g)
51
96
0
0
反应后质量(g)
x
0
88
54
下列说法中不正确的是()
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
相关试题

