【题目】元素周期表是化学学习的重要工具,依据下表回答问题:
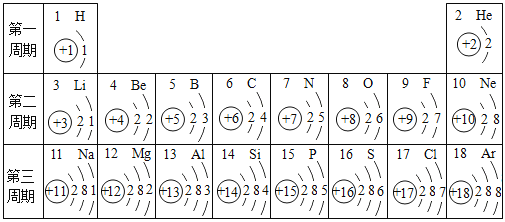
(1)表中12号元素属于 (填“金属”或“非金属”)元素,在化学反应中比较容易 (填“失去”或“得到”)电子,形成 (填离子符号).
(2)由11号元素与16号元素组成的常见化合物的化学式 .
(3)表中同一周期原子的核外电子排布规律是 .
参考答案:
【答案】(1)金属,失去,Mg2+;(2)Na2S;(3)从左至右最外层电子数依次增大.
【解析】
试题分析::(1)由12号元素在元素周期表的信息可知属于金属元素,原子结构示意图可知它的最外层有2个电子,故在化学反应中易失去电子达到稳定结构,形成带两个单位这个电荷的镁离子;(2)依据化合价书写化学式,由11号元素为钠,化合价为+1价,16号元素为硫,化合价为﹣2,故硫化钠的化学式:Na2S;(3)根据元素周期表中规律的知识可知元素周期表中同一横行元素从左至右最外层电子数依次增大
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关催化剂的说法正确的是( )
A. 在化学反应后其质量减小 B. 催化剂只能加快化学反应速率
C. 一个反应的催化剂可以有多种 D. 在化学反应后其性质一定不发生改变
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B是金属氧化物,如图所示是各物质之间的相互转化关系.请回答:
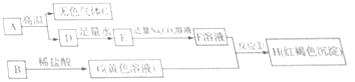
(1)写出下列物质的化学式:B ;D .
(2)反应①的化学方程式为 .
(3)举出E在农业生产中的一种用途 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】质量守恒定律是化学反应中的重要规律,我能运用此规律解答下列问题:
(1)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+3O2=2CO2+3H2O(反应条件已略去),则X的化学式为 .
(2)在催化剂并加热的条件下,A与B反应生成C和D.反应前后分子变化的微观示意图所下所示:
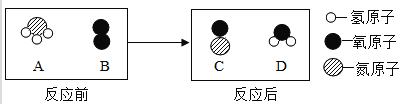
①下列说法正确的是 (填序号).
a.该反应类型为置换反应
b.4种物质中只有D属于氧化物
c.反应前后,氮元素化合价升高
d.化学反应中分子可以再分,而原子不能
②该反应的化学方程式为 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学在实验室发现一瓶由碳酸钠和氯化钠组成的混合溶液.为了测定该混合溶液中碳酸钠的质量分数,该同学设计了如下实验:取该混合溶液50g,向其中逐滴加入稀盐酸,当加入盐酸的质量为15g、30g、45g、60g时,生成气体的质量见下表(气体的溶解度忽略不计).
第Ⅰ组
第Ⅱ组
第Ⅲ组
第Ⅳ组
稀盐酸的质量/g
15
30
45
60
生成气体的质量/g
1.8
n
4.4
4.4
(1)第Ⅱ组数据n为 g.
(2)混合溶液中碳酸钠的质量分数是多少?(写出计算过程,结果精确至0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
R
O2
CO2
H2O
反应前质量(g)
51
96
0
0
反应后质量(g)
x
0
88
54
下列说法中不正确的是()
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列数型图像回答:

(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线。向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为 (填离子符号)
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系
①由图可知中和反应是放热反应,你的依据为
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为
(3)图三是a、d、c三种物质的溶解度曲线。a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用 的方法达到饱和状态
②将t2℃时,150g a物质的饱和溶液降温到t1℃时。可以析出 g a物质。
(4)下图托盘天平两边是等质量的铁和镁分别跟等质量等浓度的稀硫酸反应,反应时间t与生成氢气质量m的变化关系如图四。
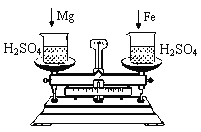
试回答:从开始反应到不再产生气体为止,天平指针偏转情况是
相关试题

