【题目】化学兴趣小组的同学将足量的锌粒加入到某未知浓度硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究。
已知,锌与稀硫酸反应的化学方程式__________
(提出问题)锌粒加入某未知浓度硫酸后生成的气体是什么?
(查阅资料)
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③H2+CuO![]() Cu+H2O
Cu+H2O
(提出猜想)
甲:气体是H2 ; 乙:气体是SO2 ; 丙:气体是SO2和H2 。
(实验探究)
为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:

(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有________。
(2)C装置在点燃酒精灯加热之前应先通一段时间的气体,加热一段时间后,观察到______,证明气体中含有H2。
(讨论)
(1)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?
用文字简述原因:_________。
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是____(任填一种合理的答案)。
参考答案:
【答案】Zn+H2SO4=ZnSO4+H2↑ SO2 C中黑色固体变红 随着反应进行,浓硫酸逐渐被消耗,导致其浓度逐渐变小 不会产生有害气体,更环保(合理即可)
【解析】
锌与稀硫酸反应生成了硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
实验探究:
(1)由于SO2能使品红(一种红色色素)溶液褪色,由题意可知,实验开始后,观察到A中品红溶液褪色,证明气体中含有 SO2;
(2)由于氢气具有还原性,能将氧化铜还原为铜,所以C装置在点燃酒精灯加热之前应先通一段时间的气体,加热一段时间后,观察到C中黑色固体变红,证明气体中含有H2;
讨论:
(1)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气,原因是:随着反应进行,浓硫酸逐渐被消耗,导致其浓度逐渐变小,稀硫酸能与锌反应生成了氢气;
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是不会产生有害气体,更环保等。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是实验室制备气体的常用装置,请回答下列问题。

(1)写出仪器a的名称___________
(2)请从上述装置中选出实验室制取干燥氧气的一组发生和收集装置____________(填字母),该反应的化学方程式是_____________。
(3)用B装置为发生装置制取CO2时,其优点是______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“页岩气”是蕴藏在岩层中的天然气,被誉为未来能源的“明星”。
(1)天然气属于不可再生能源。为缓解能源危机,人们正积极开发利用新能源,下列属于新能源的是________
a.煤 b、石油 c、氢能 d、风能
(2)天然气是重要的化石燃料,其主要成分甲烷可通过以下方式制得:将二氧化碳和氢气在催化剂作用下,生成甲烷和氧气。该反应的化学方程式是_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、B、C、D为初中化学常见的四种物质,A、B、C、D中均含有一种相同的元素,常温下,A为无色液体,C为黑色固体,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)

(1)A的化学式为__________,
(2)C与D发生的化学反应___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验设计不能达到其对应实验目的是( )
A. 测定空气里氧气的含量
 B. 生成炭黑的实验
B. 生成炭黑的实验
C. 验证质量守恒定律
 D. 比较空气与人体呼出的气体中CO2含量
D. 比较空气与人体呼出的气体中CO2含量
-
科目: 来源: 题型:
查看答案和解析>>【题目】汉黄芩素(C16H12O5)是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述不正确的是( )
A. 汉黄芩素由碳、氢、氧三种元素组成
B. 汉黄芩素中碳氧元素的质量比为12:5
C. 汉黄芩素在氧气中完全燃烧生成二氧化碳和水
D. 汉黄芩素中含有16个碳原子,12个氢原子和5个氧原子
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有以下曲线,与之对应的叙述正确的是( )
A. 用氯酸钾制取氧气
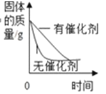
B. 加热一定质量的高锰酸钾固体

C. 在密闭容器中用红磷测定空气中氧气的含量
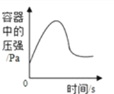
D. 发生的反应为:2KNO3
 2KNO2+O2↑
2KNO2+O2↑
相关试题

