【题目】现有下列几种常见实验装置
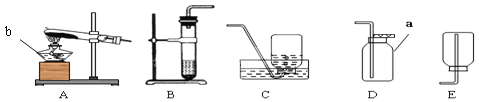
(1)写出图中有标号仪器的名称:a___________、b___________;
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是_________(填字母),其反应的文字(符号)表达式是___________________________,该反应所属的基本反应类型是____________。(填“化合反应”或“分解反应”)
(3)写出用高锰酸钾制取氧气的文字(符号)表达式为______________________________________。根据该反应原理,可选择图中__________(填字母)组装一套制取和收集纯净氧气的装置,组装仪器时在该装置试管口处添加了一团棉花,其目的是 __________________________________。
(4)用D装置收集氧气的依据是____________,检验氧气是否集满的方法是____________________。
(5)采用分解过氧化氢溶液制取氧气的优点___________(填序号).
①产物无污染 ②不需加热 ③生成物只有氧气
参考答案:
【答案】 酒精灯 集气瓶 B 过氧化氢![]() 水+氧气(H2O2
水+氧气(H2O2![]() H2O+O2) 分解反应 高锰酸钾
H2O+O2) 分解反应 高锰酸钾![]() 锰酸钾+二氧化锰+氧气(KMnO4
锰酸钾+二氧化锰+氧气(KMnO4![]() K2MnO4+MnO2+O2) AC 防止加热时高锰酸钾粉末进入导管 氧气密度比空气略大且不与空气成分反应 【答题空10】将带火星的木条放在集气瓶口,若复燃,则已满 ① ②
K2MnO4+MnO2+O2) AC 防止加热时高锰酸钾粉末进入导管 氧气密度比空气略大且不与空气成分反应 【答题空10】将带火星的木条放在集气瓶口,若复燃,则已满 ① ②
【解析】(1)酒精灯是常用的加热仪器,集气瓶是常用的收集仪器;(2)用双氧水和二氧化锰制氧气就不需要加热,可选用的发生装置是B;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的文字(符号)表达式是:过氧化氢![]() 水+氧气(H2O2
水+氧气(H2O2 ![]() H2O+O2),反应物是一种,生成物是两种,属于分解反应;(3)高锰酸钾制取氧气的文字(符号)表达式为:高锰酸钾
H2O+O2),反应物是一种,生成物是两种,属于分解反应;(3)高锰酸钾制取氧气的文字(符号)表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气(KMnO4
锰酸钾+二氧化锰+氧气(KMnO4![]() K2MnO4+MnO2+O2);用高锰酸钾制氧气就需要加热,可选用的发生装置是A,收集纯净氧气的装置应用排水法收集;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;(4)氧气的密度比空气的密度大且不与空气成分反应,因此能用向上排空气法;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;(5) 采用分解过氧化氢溶液制取氧气的优点是:不需要加热、操作简便、无污染等。
K2MnO4+MnO2+O2);用高锰酸钾制氧气就需要加热,可选用的发生装置是A,收集纯净氧气的装置应用排水法收集;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;(4)氧气的密度比空气的密度大且不与空气成分反应,因此能用向上排空气法;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;(5) 采用分解过氧化氢溶液制取氧气的优点是:不需要加热、操作简便、无污染等。
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有氧气、硫酸铜溶液、铁、碳酸钙四种物质,从中选择合适的物质作反应物,按以下要求各写一个化学方程式。
(1)分解反应:_________________________。
(2)化合反应:_________________________。
(3)置换反应:_________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】日本曾向美国借了331公斤武器级钚,至今赖着不还,钚除用于核电外,还可用于制造核武器,现在日本已是世界第六大钚贮存国。钚元素的有关信息如图,下列说法正确的是( )
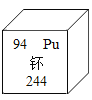
A. 钚原子中有94个中子 B. 钚原子核外有150个电子
C. 钚的相对原子质量是244g D. 钚是金属元素
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据图实验回答问题。
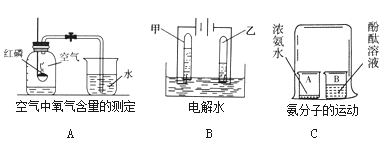
(1)A实验中白磷燃烧的文字(符号)表达式:____________________________________实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是_______________________(填一条即可)。该实验不能用木炭代替红磷,理由是________________________________________。
(2)B实验中发生反应的文字(符号)表达式:___________________________;乙试管中产生气体的名称是________.
(3)C实验中,无色的酚酞溶液变成红色.由此说明分子具有的性质是__________________;浓氨水具有的物理性质是______________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白.
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂.
【实验验证】
实验步骤
实验现象
实验结论
实验一
_______________
有少量气泡
木条不复燃
常温下过氧化氢溶液分解速率很慢.
实验二
在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中
________
氧化铝能加快过氧化氢的分解速率
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究_______________________________________ 。
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行__________,洗涤,干燥,称量;④对比反应前后氧化铝的质量.
【交流讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究_____________________________________ 。
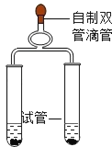
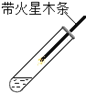
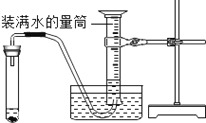
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铝对过氧化氢溶液分解的催化作用,其中观察效果最差的_________
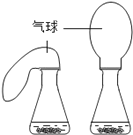
第一组
第二组
第三组
第四组
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
-
科目: 来源: 题型:
查看答案和解析>>【题目】“微观﹣宏观﹣符号”三重表征是化学独特的表示方法.
(1)根据下图回答相关问题:
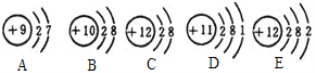
①微粒A最外层电子数是______,在化学反应中容易_____(填“得”或“失”)电子;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是_____(填字母,下同),属于同一种元素的是________和________
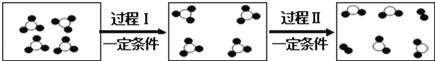
(2)如图是某密闭容器中物质变化过程的微观示意图(其中:“●”代表氧原子,“○”代表硫原子),其中发生化学变化的是过程______(填“Ⅰ”或“Ⅱ”)。
(3)用化学符号和数字填空:①7个氮原子__________ ;②3个钠离子_________
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类的生活和工农业生产都离不开水。下图是自来水厂净水过程示意图。
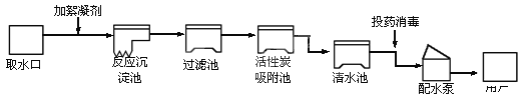
请根据图示回答下列问题:
(1)自来水厂生产自来水时,加入絮凝剂明矾的作用是_______________________ 。
(2)上图吸附池内的活性炭起________作用,经沉淀、过滤等净化处理后所得的水_______纯水(填“是”或“不是”)。
(3)家庭生活中可以用___________检验某水样是硬水还是软水。长期饮用硬水对人体不利,要降低水的硬度,生活中可采用______________的方法。
(4)有些科学家预言:“世界上最后一滴水就是人类的眼泪”。这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染。请你举一例节约用水的做法____________________。
相关试题

