【题目】实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入溶质质量分数为26.5%的碳酸钠溶液,测得溶液pH随加入碳酸钠溶液质量的变化曲线如下图所示。
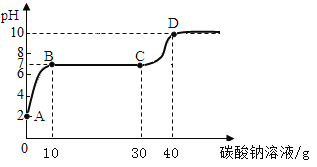
回答下列问题:
⑴A点处溶液中溶质的化学式是CaCl2和______________;
⑵计算原滤液中氯化钙的质量分数为_____________(写出计算过程,结果精确到0.1%)。
⑶根据计算所得数据在下图中画出产生沉淀的曲线。
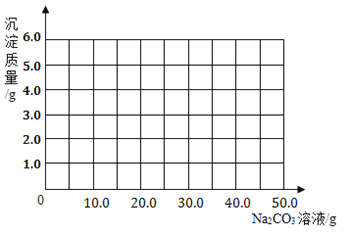 _______________
_______________
⑷CD段pH上升的原因是________________________________。
参考答案:
【答案】 HCl 11.1% 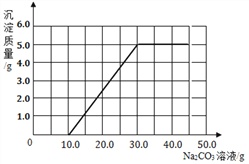 加入Na2CO3溶液增多,pH升高
加入Na2CO3溶液增多,pH升高
【解析】本题考查了根据化学反应方程式的计算和有关溶质质量分数的计算。弄清反应过程是解题的关键。
(1)稀盐酸和大理石反应生成氯化钙、水和二氧化碳,溶液中还有过量的盐酸,所以A点处溶液中溶质的化学式是CaCl2和HCl;
(2)从图中看出Na2CO3会先与盐酸反应,所以溶液的pH逐渐变大,再与CaCl2反应,BC段是CaCl2与Na2CO3反应;与CaCl2反应的Na2CO3溶液的质量为(30g-10g)=20g ;
设:滤液中CaCl2的质量为x,生成碳酸钙的质量为y。
CaCl2+Na2CO3═CaCO3↓+2NaCl,
111 106 100
x 20g×10.6% y
![]() x=5.55g,
x=5.55g,
滤液中CaCl2的质量分数=![]() ×100%=11.1%,
×100%=11.1%,
答:滤液中CaCl2的质量分数为11.1%。
(3)![]() y=5g;根据计算所得数据在下图中画出产生沉淀的曲线如图所示:
y=5g;根据计算所得数据在下图中画出产生沉淀的曲线如图所示: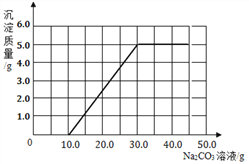
(4)图中CD段表示的意义是反应结束,碳酸钠溶液过量,碳酸钠溶液呈碱性,溶液的碱性增强,CD段pH上升的原因是加入Na2CO3溶液增多,pH升高。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(本题的所有夹持仪器均已省略)请根据下图回答问题:
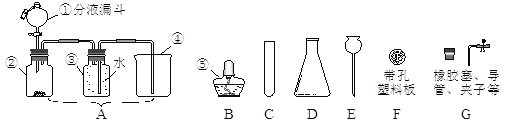
⑴ 图中仪器⑤的名称:⑤____________。
⑵ 实验室制取氧气,周颖同学设计了图A的装置,并用仪器③收集氧气。其中,仪器①中盛放的试剂名称应为_________,此法生成氧气的化学方程式为________________,收集氧气的方法为___________。
⑶ 实验室制取二氧化碳,从B~G中选择仪器,组装发生装置,要求能方便控制反应的发生或停止,你的选择为__________(填字母),反应的化学方程式为__________________。若用下图装置进行“排空气法”收集制取的CO2,请把图中的“导气管”补画完整。
 ________________
________________⑷ 下图是氢气还原氧化铁的微型实验装置图。其中“微型塑料滴管”的作用相当于上图A实验装置中的____________(填仪器编号);用微型仪器进行实验,具有的优点是___________________(写1点)。
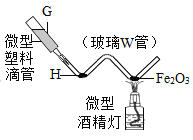
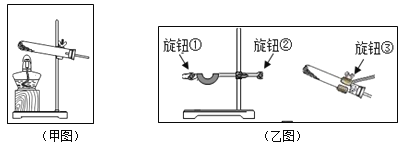
⑸ 如下甲图是周颖同学组装的另一套制O2装置,但她发现试管固定得太高,此时她应调节乙图中的旋钮____________(填①或②或③)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】兴趣小组同学为了弄清即将维修的沼气池中气体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,再用木棍拨动使瓶中的水全部倒出(见图),然后迅速拉起矿泉水瓶,盖上瓶盖。

这种方法属于____________集气法。
【对气体猜想】猜想Ⅰ:全部是CH4; 猜想Ⅱ:全部是CO;
猜想Ⅲ:全部是CO2; 猜想Ⅳ:是CH4和CO2的混合气体。
【实验和推断】

⑴若“现象a”为石灰水变浑浊,则说明气体中含有_____气体。
⑵步骤②的目的是____________________________________;步骤③“注水装置”应选下图中的____________(填序号)。

⑶若“现象b”为杯壁有水雾出现,有同学认为“猜想Ⅰ或Ⅳ”成立,其反应方程式为:____________; 另有同学认为此现象不能证明收集到的气体中一定含有氢元素,理由是_______________;要排除这种干扰可采取的措施是______________________________。
⑷ 采取⑶中的排除干扰措施后:若“现象a、b”为无明显现象,“现象c”为石灰水变浑浊,则证明“猜想_________”成立;若“现象a、c”均为石灰水变浑浊,“现象b”为杯壁有水雾,则证明“猜想__________”成立。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国女科学家屠呦呦获2015年诺贝尔生理学或医学奖。她最初的发现,让青蒿素(化学式:C15H22O5)成为世界卫生组织推荐的一线抗疟药,挽救了全球数百万人的生命。而下图是某厂生产的青蒿素的说明书部分内容。
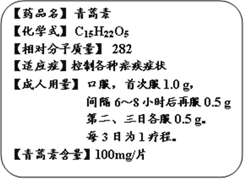
⑴青蒿素属于____________化合物(填“有机”或“无机”)
⑵青蒿素含有____________种元素;碳、氧的原子个数比为____________(填最简比)。
⑶青蒿素中氢元素的质量分数是_________(精确到0.1%)。
⑷用青蒿素控制疟疾症状一般以三天为1个疗程。根据图中说明,一个成人疟疾患者在一个疗程中共需服该药物____片。
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下图所示。
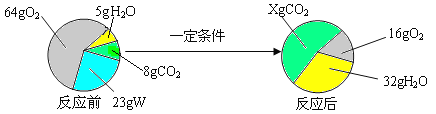
下列关于以上反应的说法中,正确的是
A. X的值为44 B. W由碳、氢两种元素组成
C. 该反应属于置换反应 D. W中碳、氢元素质量比为4∶1
-
科目: 来源: 题型:
查看答案和解析>>【题目】氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示,请结合图表数据回答下列问题:
氢氧化钠
碳酸钠
20℃
40℃
20℃
40℃
水
109g
129g
21.8g
49g
酒精
17.3g
40g
不溶
不溶
(1)下图表示________(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
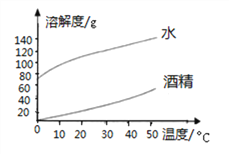
(2)温度从20℃升到40℃时,氢氧化钠在水中的溶解度变化__________(填“大于”或“小于”)碳酸钠在水中的溶解度变化。
(3)40℃ 时,若将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的溶剂是__,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为______________。
(4)若要对比两种固体物质的溶解性,必须在_____________、______________ 、_____________的条件下进行对比。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图表示四种液体或溶液中存在的粒子示意图。(图中粒子个数不代表实际粒子数目关系)
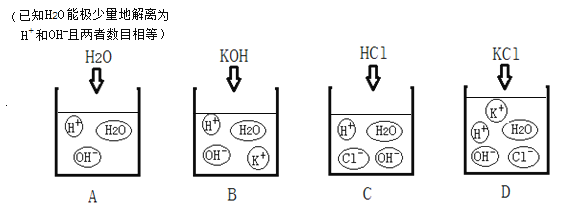
请回答。
(1)在烧杯A、B、C中分别滴入2-3滴酚酞溶液,烧杯______(填字母编号)的溶液变红。
(2)若烧杯D的溶液是另取一定量的烧杯B、C 中的溶液混合后得到的,再向其中滴入酚酞溶液不变红,小明推断是氢氧化钾与盐酸恰好完全反应了。小红则提出该推断_____(填“正确”或“不正确”),理由是_____________________。烧杯D 中水分子的数目一定______(填“大于”或“等于”或“小于”)烧杯B、C中的水分子数目之和。
(3)四个烧杯中能证明使酚酞变红的粒子不是K+的是_____________________(填字母编号)。
依据烧杯A、B、C中滴入酚酞溶液后的现象,请从微观角度解释酚酞溶液遇液体或溶液变红的原因是_______________________________。
相关试题

