【题目】取10.9g纯碱样品(含少量氯化钠杂质)完全溶于108.8g水中,再向其中逐滴加入100g溶质质量分数为20.8%的氯化钡溶液,恰好完全反应,所得溶液为不饱和溶液,请根据题意回答下列问题:
(1)100g溶质质量分数为20.8%的氯化钡溶液中氯化钡的质量为__g;
(2)完全反应后所得溶液中溶质的质量分数为多少_______? (写出计算过程)。
参考答案:
【答案】 20.8 6%
【解析】本题主要考查运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力。
(1)氯化钡溶液中氯化钡的质量为:100g×20.8%=20.8g;
(2)设:纯碱样品中Na2CO3的质量为x,生成NaCl的质量为y,生成碳酸钡沉淀质量为z,
Na2CO3 +BaCl2=BaCO3↓+2NaCl
106 208 197 117
x 20.8g z y
![]() 解得:x=10.6g;
解得:x=10.6g;
![]() 解得:y=11.7g;
解得:y=11.7g;
![]() 解得:z=19.7g;
解得:z=19.7g;
完全反应后所得溶液中溶质的质量分数为:![]() ×100%=6%;
×100%=6%;
答:氯化钡溶液中氯化钡的质量为20.8g;
完全反应后所得溶液中溶质的质量分数为6%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】共享单车采用手机扫描二维码来解锁,而手机通常采用高能的锂(元素符号为Li)电池作为电源。
(1)锂原子的原子结构示意图如图所示
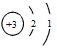 ,在化学反应中容易______而成为锂离子,其离子符号为______。
,在化学反应中容易______而成为锂离子,其离子符号为______。(2)某种锂电池放电时的总反应为Li+MnO2=LiMnO2。LiMnO2中锰元素的化合价为__________。
(3)金属锂除了制造锂电池外,还可以用于储存氢气,其原理是金属锂与氢气化合生成白色粉末状的氢化锂(LiH),氢化锂与水反应生成氢氧化锂和氢气。写出氢化锂与水反应的化学方程式___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A﹣H均为初中化学常见的物质,其中A、C常温下是气体,且组成元素相同,C的固体俗名叫“干冰”,B是赤铁矿的主要成分,E能用于改良酸洗土壤,H是紫红色金属。他们的相互转化关系如图(图中反应条件均已略去):
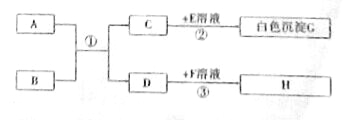
请回答下列问题:
(1)写出E物质的化学式 。
(2)写出反应①的化学方程式 。
(3)反应③的基本反应类型是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学利用下图装置制取并收集一瓶二氧化碳气体,请和他们一起完成以下实验探究。

(1)写出标号①的仪器名称__________。
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为__________(填序号),反应的化学方程式为__________。
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】 废液中的溶质含有哪些物质?
【查阅资料】 氯化钙溶液呈中性。
【猜想与假设】 猜想①:废液中的溶质只有氯化钙;
猜想②:废液中的溶质是氯化钙和__________(填化学式)。
【设计并进行实验】 I.为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合适的一种进行实验,证明了猜想②是正确的。他们选择的药品不可能是__________。
A.紫色石蕊试液 B.无色酚酞试液 C.锌粒 D.氧化铁粉末 E.氢氧化钠溶液
Ⅱ.乙小组用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的实验报告。
实验操作
实验现象
实验结论
取少量反应后的废液于试管中,加入足量_______(填化学式)溶液,振荡。
____________
猜想②正确
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行处理,实行无害化排放,从源头上消除对环境的污染。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了达到相应的实验目的,下列实验设计部不合理的是
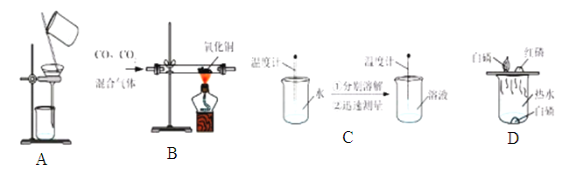
A.分离H2O2和MnO2制O2后的固液混合物 B.除去CO中的CO2气体
C.区分NaCl、NH4NO3、NaOH三种固体 D.探究可燃物燃烧的条件
-
科目: 来源: 题型:
查看答案和解析>>【题目】图一是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图二是30℃时,取其中两种固体各1g分别放进盛有10g水的两只试管中,充分振荡后的溶解情况。下列说法正确的是
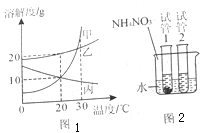
A.甲物质的溶解度比乙物质的溶解度大
B.加入试管1的固体是丙
C.向烧杯中加入硝酸铵固体后,试管2中一定有晶体析出
D.将30℃时甲、乙、丙三种物质的饱和溶液降温到20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
-
科目: 来源: 题型:
查看答案和解析>>【题目】往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是
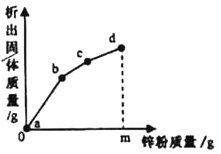
A. bc段(不含两端点)析出的金属是Fe
B. c点对应溶液中含有的金属离子为Zn2+和Cu2+
C. ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+、Fe2+
D. 若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,m1>m2
相关试题

