【题目】某化学兴趣小组的同学利用下图装置制取并收集一瓶二氧化碳气体,请和他们一起完成以下实验探究。

(1)写出标号①的仪器名称__________。
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为__________(填序号),反应的化学方程式为__________。
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】 废液中的溶质含有哪些物质?
【查阅资料】 氯化钙溶液呈中性。
【猜想与假设】 猜想①:废液中的溶质只有氯化钙;
猜想②:废液中的溶质是氯化钙和__________(填化学式)。
【设计并进行实验】 I.为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合适的一种进行实验,证明了猜想②是正确的。他们选择的药品不可能是__________。
A.紫色石蕊试液 B.无色酚酞试液 C.锌粒 D.氧化铁粉末 E.氢氧化钠溶液
Ⅱ.乙小组用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量反应后的废液于试管中,加入足量_______(填化学式)溶液,振荡。 | ____________ | 猜想②正确 |
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行处理,实行无害化排放,从源头上消除对环境的污染。
参考答案:
【答案】(1)铁架台。(2)B, CaCO3 + 2HCl == CaCl2 + H2O + CO2↑。(3)HCl BE,Zn 或Fe2O3,
产生气体或溶液变成黄色;Zn+2HCl==ZnCl2+H2↑;或Fe2O3+ + 6HCl == 2FeCl3 + 3H2O
【解析】(1)铁架台。(2)选择发生装置需考虑是因素是,反应物的状态和反应条件。加热固体制取气体,发生装置为A,固体和液体常温下反应制取气体应选用的发生装置为B;实验室常用石灰石和稀盐酸制取二氧化碳气体,应选用固液常温型收集装置B,反应的化学方程式为CaCO3 + 2HCl == CaCl2 + H2O + CO2↑。(3)由反应方程式可知,但石灰石和稀盐酸刚好完全反应时溶质是氯化钙;但盐酸过量时溶质是氯化钙和氯化氢;验证反应后溶液中的溶质时,由于生成物一定存在,所以不需要验证,需要验证的是可能存在的过量的反应物。所以要确认反应后溶质的成分,需要验证的是盐酸。盐酸能使紫色石蕊试液变红,不能使无色酚酞变色;和锌反应有气体生成,反应方程式为;Zn+2HCl==ZnCl2+H2↑;和氧化铁反应得到黄色溶液;反应方程式为:Fe2O3+ + 6HCl == 2FeCl3 + 3H2O和氢氧化钠反应无明显现象,所以不能用酚酞试液、氢氧化钠溶液验证盐酸是否存在。
-
科目: 来源: 题型:
查看答案和解析>>【题目】鞋垫中填充有活性炭,主要利用该物质的
A.吸附性 B.稳定性 C.可燃性 D.还原性
-
科目: 来源: 题型:
查看答案和解析>>【题目】遂宁市大英县境内郪江河畔的“中国死海”,是北纬30度上又一神奇的景观。
(1)“中国死海”中天然盐卤水的溶质以氯化钠为主,并富含钾、钙、碘、溴等40多种矿物质和微量元素,对人体健康起到非常重要的改善和调节作用。碘元素在元素周期表中的信息和原子结构示意图如下,下列说法正确的是________。
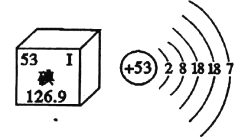
A.碘的相对原子质量为126.9 g B.人体缺碘易导致骨质疏松
C.碘在化学反应中形成的阴离子符号为I— D.一个碘原子核内有53个中子
(2)“中国死海”的现代水上运动、休闲、度假、娱乐、保健等水文化旅游元素提升了人们的生活品质,但也容易对郪江造成污染。请提出一条保护水资源的建议__________。
(3)小西同学从郪江中取少量水样,观察到水样浑浊,有固体小颗粒。为除去这些不溶性杂质,她应该采取实验操作的名称是___________。
(4)浩瀚的海洋中蕴藏着丰富的资源,是巨大的天然宝库。从海水中提取溴,其中一种方案涉及到的化学反应为:2NaBr+Cl2=2NaCl+Br2,已知非金属单质也有类似金属单质与盐溶液之间的反应规律,由此可判断Cl2、Br2的活动性顺序是:Cl2_______Br2(填“>”、“<”或“=”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】冬季室内燃煤取暖时,要注意通风,以免造成人员中毒。这里的有毒气体主要是指
A.O2 B.N2 C.CO D.CO2
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图。
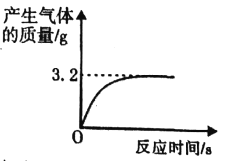
(1)完全反应后,经过滤、烘干,得到固体的质量为_______(不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是_______。
A.二氧化锰越来越少
B.过氧化氢溶液的溶质质盘分数越来越小
D.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数。(规范写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列属于纯净物的是
A.食醋 B.干冰 C.硬水 D.石灰水
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列反应的化学方程式正确的是
A.铁在氧气中燃烧: 2Fe +3O2
 2Fe2O3
2Fe2O3B.硫酸铵与烧碱混合: ( NH4 ) 2 SO4 +2NaOH=Na2SO4 +2H2 O +2NH3 ↑
C.铝片放入硝酸银溶液中: Al + AgNO3=AlNO3 + Ag
D.向氯化镁溶液中滴入硫酸钾溶液: MgCl2 + K2 SO4=MgSO4 ↓ + 2KCl
相关试题

