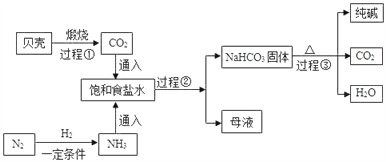
【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:
(小资料)
I、贝壳的主要成分是 CaCO3
Ⅱ、通常情况下,1 体积水中大约能溶解 700 体积氨气,1 体积水中大约能溶解 1 体积二氧 化碳
Ⅲ、饱和食盐水中发生的主要反应为: NH3+CO2+H2O=NH4HCO3, NH4HCO3+NaCl=NaHCO3↓+NH4Cl(NaHCO3 是因为饱和后析出,变成沉淀)。
(1)合成氨需要的氮气来自空气,空气属于______填“混合物”或“纯净物”).空 气中氮气的体积分数约为_____。
(2)过程②中主要操作的名称是_____。
(3)过程①中发生反应的化学方程式为 _____,过程③中反应所属基本反应基本类型为__________。
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入_____(填“NH3” 或“CO2”),你的理由是:_____。
(5)上述流程中可以循环利用的物质是:_____(填化学式)。
参考答案:
【答案】 混合物 78%; 过滤; CaCO3![]() CaO+CO2↑ 分解反应; NH3 因为氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有 利于生成较多的碳酸氢钠 CO2.
CaO+CO2↑ 分解反应; NH3 因为氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有 利于生成较多的碳酸氢钠 CO2.
【解析】根据所学知识和题中信息知,Ⅲ、(1)合成氨需要的氮气来自空气,空气属于混合物,空气是一种典型的混合物。空气中氮气的体积分数约为78%。(2)过程②中主要操作的名称是过滤,把不溶于液体的固体物质与液体分离的一种方法。(3)过程①中发生反应的化学方程式为CaCO3![]() CaO+CO2↑,过程③中反应所属基本反应基本类型为分解反应,一种物质分解生成了三种物质。(4)为了提高产率,往饱和食盐水中通入气体时,应该先通入NH3,理由是因为氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有利于生成较多的碳酸氢钠。(5)上述流程中可以循环利用的物质是CO2。
CaO+CO2↑,过程③中反应所属基本反应基本类型为分解反应,一种物质分解生成了三种物质。(4)为了提高产率,往饱和食盐水中通入气体时,应该先通入NH3,理由是因为氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有利于生成较多的碳酸氢钠。(5)上述流程中可以循环利用的物质是CO2。
点睛∶空气是一种典型的混合物。空气主要成分是氧气和氮气,氮气的体积分数约为78%,氧气的体积分数约为21%。分解反应的基本特征是一变多。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合图 1(A 至 E)回答问题:
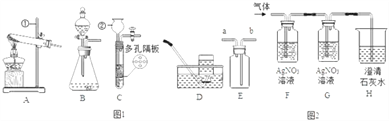
(1)仪器名称:①__________________,②________________;
(2)用氯酸钾和二氧化锰制取氧气,可选用装置____________(选填序号)和 D 组合,反 应的化学方程式为_____________________, 二氧化锰的作用是_______;
(3)实验室可用装置 B 或 C 制 H2,C 装置相对于 B 的优点有_____。用 E 装置用排空气法收集 H2,气体应从_____(选填“a”或“b”)端通入;
(4)有同学将实验室制得的 CO2 通入澄清石灰水,石灰水未变浑浊,于是将气体通往图 2(F 至 H)装置进行探究:
①实验室制 CO2 反应的化学方程式______________________________;
②装置 F、H 中溶液变浑浊,G 中溶液不变浑浊,则原石灰水未变浑浊的原因 是_____;
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示某些物质间的转化关系(反应条件均略去),其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属,B、D、E均为无色气体.请回答:
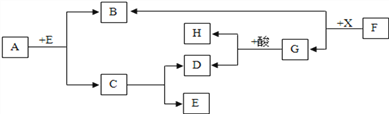
(1)X是________或________。D是____________。(填化学式)
(2)B物质固态时的名称是________。
(3)写出下列反应的化学方程式
①A+E→B+C:_________________________________.
②G与E在一定条件下反应的化学方程式: ________ .
-
科目: 来源: 题型:
查看答案和解析>>【题目】你玩过拼图吗?以下拼图分别代表Fe、CO2、H2SO4、Ca(OH)2、BaCl2、Cu (NO3)2中的一种物质,其中③是同类物质中年产量最多的一种材料,规则是能反应的物质可以邻边相接拼在一起。
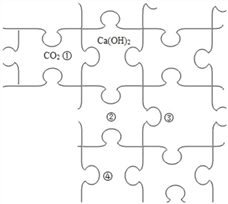
(1)H2SO4应安排在位置____________(填序号)
(2)图中CO2和相邻物质发生反应的现象为____________________。
(3)写出②和③反应的化学方程式_________________,该反应的基本类型是__________。
(4)请写出一种能放在③④夹角间空拼图处的一种无色盐溶液的溶质化学式_______________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验.实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加,结合题目信息,回答以下问题:
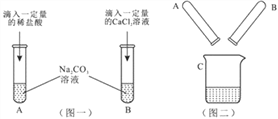
(1)甲同学的实验完成后,A试管一定有剩余的物质是_________。
(2)B试管的实验发生的化学方程式是________________。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是_______。。
猜想三:滤液中的溶质是NaCl、CaCl2、Na2CO3
猜想四:滤液中的溶质是NaCl
【讨论与交流】通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)你认为不合理的猜想是_______,理由是______。
【进行实验】丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是_________。
【实验结论】通过探究,小组同学得出了猜想一成立的结论。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在教育创强活动中,很多学校都加大投入改善硬件设施,一种新型环保材料被塑 胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(其化学式为C15H10N2O2)。请回答下列有关问题;
(1)二甲苯烷二异氰酸酯(C15H10N2O2)由_____种元素组成,氢、氧元素的质量比为_____(填最简整数比)。
(2)二甲苯烷二异氰酸酯(C15H10N2O2)的相对分子质量为_____。
(3)500g 二甲苯烷二异氰酸酯中含氮元素的质量为_____g.
-
科目: 来源: 题型:
查看答案和解析>>【题目】将40g稀盐酸逐滴加入到20g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐酸的滴加,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中热量损失)。试回答:
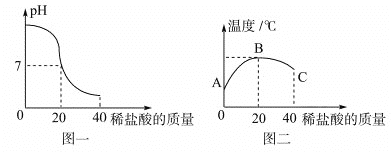
(1)图二从A到B过程中,溶液的pH逐渐__________(填“增大”或“减小”)。
(2)图二表示酸碱恰好完全反应的点是___________。
(3) 向图二C点处的溶液中滴加紫色石蕊试液,溶液显_______ 色。
(4)计算稀盐酸中溶质的质量分数为__________。(写出计算过程)
相关试题

