【题目】学习化学离不开实验和科学探究。
(实验活动一)甲、乙两位同学用如图所示的装置定量测定空气中氧气的体积分数。
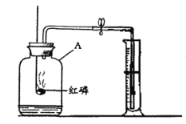
已知广口瓶中空气体积为250mL(已扣除瓶塞和瓶中水所占体积)
I.他们实验过程如下:
(1)
(2)用弹簧夹夹住橡胶管后,将燃烧匙中红磷在酒精灯上点燃后伸入集气瓶中,并将导管伸入装有l00mL水的量筒中。
(3)过一段时间后,打开弹簧夹,等到水不再进入广口瓶时,从量筒中取出导管,记录量筒中剩余水的体积。
(4)甲同学记录量筒中水的体积为55mL,乙同学记录量筒中水的体积为44mL。
Ⅱ.仔细阅读以上实验过程回答下列问题:
(1)将上述实验过程的第一步补充完整:________________________________
(2)红磷在瓶内燃烧现象是__________________________________发生反应的文字或符号表达式为___________________________
(3)甲同学测得空气中氧气的体积分数为______乙同学测出的氧气的含量______________(填偏大或偏小)
(4)导致甲同学实验结果的原因可能是___________________
①红磷的量不足 ②实验过程中,没夹紧弹簧夹
③装置未完全冷却就打开弹簧夹 ④点燃红磷后,燃烧匙伸入集气瓶中太慢
(实验交流)在老师的指导下,甲乙两位同学又重复几次该实验,测出了比较准确的数据。
甲同学提出在不改变其他条件的情况下,能否用木炭代替红磷做这个实验呢?
乙同学认为不行,原因是___________________。乙同学预先在集气瓶内加入_______反应后,用木炭做实验也收到了较好的效果。
(实验活动二)某化学兴趣小组对教材中“测定空气里氧气含量”的实验进行了大胆改进,设计如图实验方案进行,收到了良好的效果。请你回答下列有关问题:
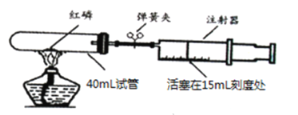
(1)活塞位置如图所示,实验前打开弹簧夹,用酒精灯加热红磷,充分反应结束后,待试管冷却,活塞前沿最终停留在_______mL的刻度线上。
(2)用该装置测定空气中氧气含量的和采用课本上的装置相比,其优点是_______________________(写一点就可以)。
参考答案:
【答案】检查装置的气密性产生大量白烟磷+ 氧气![]() 五氧化二磷18%偏大①③生成二氧化碳导致瓶内压强无法减小澄清石灰水4便于读数、误差小、减少污染等
五氧化二磷18%偏大①③生成二氧化碳导致瓶内压强无法减小澄清石灰水4便于读数、误差小、减少污染等
【解析】
实验活动一:(1)实验前先检查装置的气密性;
(2)点燃的红磷,在集气瓶燃烧,生成大量的白烟,红磷燃烧生成了五氧化二磷,红磷在瓶内燃烧的文字表达式为:磷+氧气![]() 五氧化二磷;
五氧化二磷;
(3)甲同学记录量筒中水的体积为55mL,进入集气瓶中的水为100mL-55mL=45mL,氧气的体积分数可为![]() ×100%=18%;乙同学记录量筒中水的体积为44mL,氧气的体积分数为
×100%=18%;乙同学记录量筒中水的体积为44mL,氧气的体积分数为![]() ×100%=22.4%,乙同学测出的氧气的含量偏大;
×100%=22.4%,乙同学测出的氧气的含量偏大;
(4)导致甲同学实验结果偏低的原因可能是红磷过少或装置漏气等;导致乙同学实验结果偏高的原因可能是 止水夹没有夹紧,红磷燃烧时空气外逸或燃烧匙伸入过慢,集气瓶中空气外逸;
实验与交流:因为碳粉燃烧消耗掉氧气同时又生成了二氧化碳等气体,瓶内压强基本不变,水不倒流;澄清石灰水能吸收二氧化碳,是压强减小;
实验活动二:(1)若不使用弹簧夹,用酒精灯加热红磷,红磷实际消耗掉的是试管40mL和注射器内20mL的氧气为(40mL+15mL)×![]() =11mL,所以活塞应停在15mL-11mL=4mL的刻度处;
=11mL,所以活塞应停在15mL-11mL=4mL的刻度处;
(2)从保护环境角度考虑,与用红磷燃烧的方法相比,用加热铜丝测空气中氧气含量的主要优点是不会产生五氧化二磷,污染空气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是 ( )
实
验
装
置
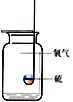
硫在氧气中燃烧
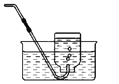
排水法收集氧气

测定空气中氧气含量
铁丝在氧气中燃烧
解释
集气瓶中的水:
吸收放出的热量
集气瓶中的水:
水将集气瓶内的空气排干净,便于观察氧气何时收集满
量筒中的水:
通过水体积的变化得出氧气体积
集气瓶中的水:
冷却溅落熔化物,防止集气瓶炸裂
A
B
C
D
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列实验装置,回答相关问题。
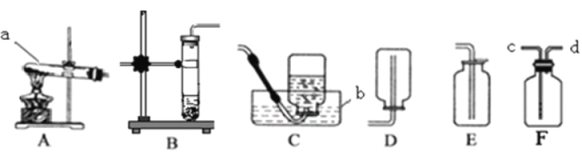
(1)写出图中标有a、b的仪器名称:a________________ b__________________。
(2)用高锰酸钾制取氧气应选择的发生装置为____________(填序号),写出该反应的文字或符号表达式__________________________。加热时试管口要略向下倾斜的原因是__________________。
(3)小李同学在用加热高锰酸钾并用排水法收集氧气的实验过程中,发现收集装置中的水慢慢变成紫红色了,他仔细思考发现反应装置中缺少_________________________,其作用是_______________。
(4)实验室利用过氧化氢溶液制取并收集较纯净的氧气,应选用的装置组合是__________,写出该反应的文字或者符号表达式_________________________。若用F装置(瓶中装满水)收集生成的氧气,气体应从____________(选填“c”或“d”)端导入。
(5)小王同学利用如图装置制取氧气并测定其密度。
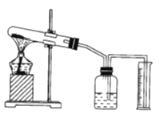
实验中测得的数据有:加热前试管和固体混合物的总质量(M克),最后量筒内增加水的体积(V毫升),为达到实验目的还需测定的数据是___________(填序号)。
A.量筒内水的质量(M1克)
B.反应完后试管内剩余固体的质量(M2克)
C .反应完后试管及管内剩余固体的总质量(M3克)。
测得氧气的密度为_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小七同学发现家里药箱中有一瓶无色液体,为了探究它是何种物质,他做了如下实验:
① 此液体编号为A,在液体A中加入蓝色溶液 C(催化剂),稍微振荡,在常温下就能迅速产生气体B,且产生了常温下为液体的纯净物D; ② 将气体B收集起来,将带火星的小木条伸入盛有气体B的集气瓶中,小木条复燃。 ③把淡黄色粉末E点燃后放入盛有气体B的集气瓶中,E能剧烈燃烧,生成一种无色有刺激性气味的气体F。④把黑色固体G点燃后伸入盛有气体B的集气瓶中,剧烈燃烧,生成使澄清石灰水变浑浊的气体H。
请根据小七的实验,回答下列问题。
(1)写出各物质的名称或化学符号:
A_______,D_______,E________,G _______。
(2)写出④中发生反应的文字或符号表达式并注明基本反应类型:__________________,____________
-
科目: 来源: 题型:
查看答案和解析>>【题目】规范实验操作是实验成功的保证,下列实验操作,其中正确的是 ( )
A. 铁丝在氧气中燃烧
 B. 取用少量液体
B. 取用少量液体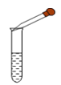
C. 加热试管中的液体
 D. 量取42mL液体
D. 量取42mL液体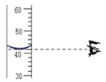
-
科目: 来源: 题型:
查看答案和解析>>【题目】(题文)(1)空气是一种宝贵的资源。
①空气成分中,作为植物进行光合作用的原料的是____________;可制成霓虹灯等电光源的气体是________。
②氮气在一定条件下可与氢气反应,生成氨气(NH3)。请写出该反应的文字表达式:________________________________。
③为了保护空气,在我国新颁布的《环境空气质量标准》中,基本监控项目增设了PM2.5浓度限值,与该监测项目有关的是__________(填字母序号)。
A.二氧化硫 B.二氧化氮 C.一氧化碳 D.可吸入颗粒物
(2)根据所学知识,完成下列填空:
①实验室做实验室时,酒精不慎洒出燃烧起来,可用_______________扑灭
②分离液态空气法制氧气:是利用氧气和氮气的_________不同进行分离的。(填“密度”或“沸点”)
③做“硫燃烧”实验时,用排水法收集气体的优点是_________
④做铁丝在氧气中燃烧的实验时,集气瓶中水的作用是__。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组利用下列装置进行实验室制取氧气,请回答:
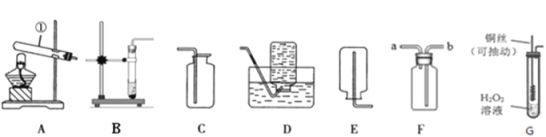
(1)指出仪器名称:①_______________
(2)实验室用氯酸钾制氧气,该反应的文字表达式为__________,可选择的发生装置为________(填字母);若改用高锰酸钾制氧气,该装置还需要做的一点改动是__________,写出该反应的文字表达式________________________。
(3)可用D装置收集氧气的理由是___________________,收集好的氧气应________(填“正”或“倒”)放在桌面上。若用F装置排空气法收集氧气,验满的方法是______________。
(4)实验改进:查阅资料发现,氧化铜可以加快过氧化氢分解的速度。现有一根洁净的铜丝,实验前先将其绕成螺旋状,再在空气中加热处理,使其表面产生黑色的氧化铜。改进后的发生装置,如图G所示(已略去支持装置)。写出该实验中涉及的反应文字表达式__________、__________________。该装置改进后与B装置相比,优点有___________
①生氧气速率更快②可通过抽动铜丝来控制氧气产生的速率
③铜丝更易回收,反复使用,节约原料 ④能得到更多的氧气
相关试题

