【题目】请结合下图回答问题:
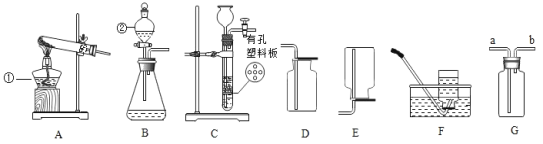
(1)写出图中有标号仪器的名称:①______,②______。
(2) 若用高锰酸钾制取氧气,应选用的发生装置是____(填字母),发生反应的化学方程式:____。实验结束后,某同学发现水槽中的水变成了紫红色,从实验操作角度分析其原因是_____;
(3)若要制取二氧化碳,反应的化学方程式为____。实验室制取CO2气体可选用B作为发生装置,与B装置相比,使用带有多孔隔板的装置C的优点是_________。
(4)若要制取氢气,可以使用 E或F 装置收集,能用E 装置收集的原因是______;若选用G装置代替E 装置收集氢气,气体应从____(填“a”或“b”)导管口通入。
(5)丽丽用家里的小针筒和废药瓶组装成一套微型装置(如图所示)来制取气体,固体只需极少 量、液体用量也很少(或只需1-2小滴),用此装置做实验的优点是____(填序号)。
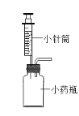
A 节约药品用量 B 能减少污染
C 能控制液体滴加的量 D 便于进行家庭实验
参考答案:
【答案】酒精灯 分液漏斗 A ![]() 试管口未放棉花
试管口未放棉花 ![]() 可控制反应的发生与停止 氢气的密度比空气小 b ABCD
可控制反应的发生与停止 氢气的密度比空气小 b ABCD
【解析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,碳酸钙与盐酸反应生成氯化钙、水、二氧化碳。
(1)仪器①为酒精灯,仪器②为分液漏斗。
(2)实验室用高锰酸钾制取氧气属于固体加热的反应,所以选用的发生装置是固固加热型,则选装置A,反应方程式为![]() ;实验结束后,某同学发现水槽中的水变成了紫红色,原因可能是试管口未放棉花,导致高锰酸钾粉末进入导管,并进入水槽,使水变成了浅紫红色。
;实验结束后,某同学发现水槽中的水变成了紫红色,原因可能是试管口未放棉花,导致高锰酸钾粉末进入导管,并进入水槽,使水变成了浅紫红色。
(3)实验室制取二氧化碳所用固体药品是大理石或石灰石,其主要成分碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,化学方程式为![]() ;B装置相比,使用带有有孔塑料板的C装 置,关闭止水夹后,管内气压增大,液面下降,直至固液分离反应停止。打开止水夹后,压强减小,液面上升,固液接触,反应继续发生。则其优点是可控制反应的发生与停止。
;B装置相比,使用带有有孔塑料板的C装 置,关闭止水夹后,管内气压增大,液面下降,直至固液分离反应停止。打开止水夹后,压强减小,液面上升,固液接触,反应继续发生。则其优点是可控制反应的发生与停止。
(4) 装置E为向下排空气法装置,能收集密度比空气小的气体。则能用E装置收集氢气,原因为:氢气的密度比空气小。使用“万用瓶”排空气法收集密度比空气小的气体,应“短进长出”所以应从b导管口通入。
(5)丽丽的微型装置用家里的小针筒和废药瓶,固体只需极少量、液体用量也很少,则其优点是节约药品用量 和能控制液体的滴加速度,同时能减少污染,便于进行家庭实验。因此,答案选ABCD。
-
科目: 来源: 题型:
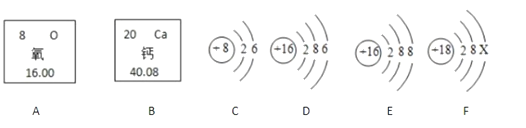
查看答案和解析>>【题目】下图中是氧元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
请你回答:
(1)氧元素的原子序数为_____。
(2)E粒子属于_____(填“原子”“阴离子”或“阳离子”),该粒子的符号为_____。
(3)F元素在元素周期表中的位置处于第_____周期
(4)写出由B、C、D三种元素组成的化合物的化学式____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系,是化学学科的特点。下图是某化学反应的微观过程示意图。
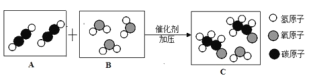
(1)请用化学符号表示图B的含义_____
(2)从微观角度说出判断物质C属于混合物的依据_____
(3)该反应的化学方程式为_____
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如下:
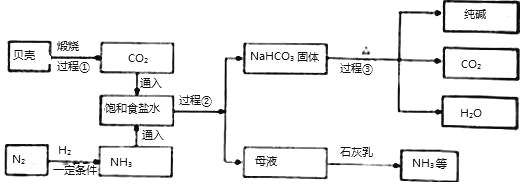
【小资料】
I、贝壳的主要成分是CaCO3
Ⅱ、通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳
Ⅲ、饱和食盐水中发生的主要反应为:NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NaHCO3↓+NH4Cl
(1)合成氨需要的氮气来自空气,空气属于 (填“混合物”或“纯净物”).空气中氮气的体积分数约为 .
(2)过程②中主要操作的名称是 .
(3)过程①中发生反应的化学方程式为 ,过程③中反应所属基本反应类型为 .
(4)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入 (填“NH3”或“CO2”),你的理由是: .
(5)上述流程中可以循环利用的物质是: (填化学式)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列是初中化学的部分实验,根据实验回答下列问题:
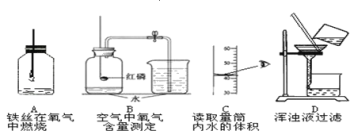
(1)A中实验前在集气瓶底部放少量水的目的是:_____;
(2)B中测得氧气的体积值偏小的原因:_____;(答一点)
(3)C实验是读取量筒中液体体积,造成的结果是:____;
(4)D实验中玻璃棒的作用是:______;
(5)要鉴别以上实验所用的水是软水还是硬水,可向自来水样品中加入适量的____,搅拌,如果观察到_______,则样品为软水。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,反应④常用于检验二氧化碳,E是一种金属氧化物,能与A反应。它们之间的转换关系如图所示:
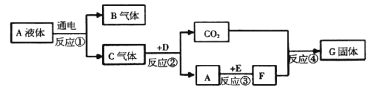
(1)写出下列物质的化学式:A_________、E_________。
(2)写出以下反应的化学方程式:
反应②______。
反应④______。
(3)E在日常生活中用途广泛,请写出其中一点_____。
(4)B与其它燃料相比其优点有________等(写一个即可)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与他们的探究并回答问题。
(查阅资料)铜和氧化铁是红色固体,铁粉是黑色固体。
(1)(提出问题)
假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是___。
(设计实验方案)同学们对实验作了如下设想和取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示)。
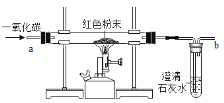
请你完成下表:
实验中可能出现的现象
结论
A红色粉末_______,石灰水_____
假设1成立
B红色粉末_________,石灰水变浑浊
假设2成立
C红色粉末部分变黑。石灰水________
假设3成立
(进行实验)通过实验及分析,确认假设3成立。
(2)(反思与评价)
①实验过程中,硬质玻璃管内发生反应的化学方程式是____。
②实验时通入一氧化碳片刻后再加热的原因是_____。
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是___。
(3)(拓展)为了把实验结束后的铜粉和铁粉分离开来,你认为可选用____(填序号)
A 过滤 B 用磁铁吸引 C 在空气中灼烧
相关试题

