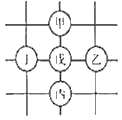
【题目】如图所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钠、碳酸钠、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中:甲一戊的反应类型不同于其它几个反应:丙一戊反应能产生一种气体。且该气体还能与丁发生反应,请回答:
(1)写出乙物质的化学式_____。
(2)写出甲一戊发生反应的化学方程式:_____。
(3)丙和丁两种物质之间可以实现双向转化,请你任选一个转化反应,写出反应的化学方程式:_____。
参考答案:
【答案】AgNO3 Fe+2HCl=FeCl2+H2↑ Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【解析】
解:(1)围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钠、碳酸钠、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应,与戊的反应中:甲一戊的反应类型不同于其它几个反应,丙一戊反应能产生一种气体,且该气体还能与丁发生反应,所以丁是氢氧化钠,丙、戊是碳酸钠和盐酸中的一种,所以戊是盐酸,丙是碳酸钠,甲是铁,铁和盐酸的反应属于置换反应,其他反应是复分解反应,所以乙就是硝酸银,经过验证,推导正确,所以乙是AgNO3;
(2)甲一戊发生复燃反应是铁和盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑;
(3)丙和丁两种物质之间可以实现双向转化,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图象能正确反映其对应关系的是( )
A.
 在一定温度下向已经饱的KNO3溶液中加入KNO3固体
在一定温度下向已经饱的KNO3溶液中加入KNO3固体B.
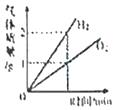 将水通电一段时间后产生气体的质量
将水通电一段时间后产生气体的质量C.
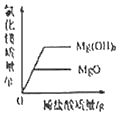 向等质量的氧化镁、氢氧化镁中,分別加入质量分数同的稀盐酸至过量
向等质量的氧化镁、氢氧化镁中,分別加入质量分数同的稀盐酸至过量D.
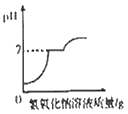 常温下向H2SO4,MgSO4混合溶液中滴加NaOH溶液
常温下向H2SO4,MgSO4混合溶液中滴加NaOH溶液 -
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置,回答问题:
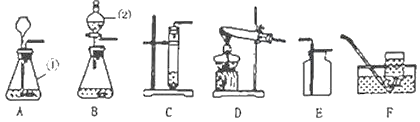
(1)写出图中标号仪器的名称:①_____,②_____。
(2)实验室用过化氢溶液和二氧化锰固体制取氧气时,发生反应的化学方程式为_____,从控制反应速率和节约药品的角度考虑,发生反应的装置最好选用_____(填装置编号)。
(3)收集氧气和二氧化碳均可以利用装置_____(填装置编号)收集,原因是_____。
(4)实验老师要把20g溶质质量分数为30%的过氧化氢溶液稀释成6%进行实验,需要加入水的质量为_____g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】山东超级工程“蓝鲸1号”在我国南海海域试采“可燃冰”成功,“可燃冰”是由天然气(主要成分为甲烷)和水在低温、高压的条件下形成的冰状固体,被科学家为“21世纪能源”,请回答下列问题:
(1)写出甲烷(CH4)完全燃烧的化学方程式_____。
(2)甲烷不仅是重要的燃料。同时也是重要的化工原料,如图是以甲烷为原料,一定条件下制取甲醇的微观过程示意图由此得出:进程1中参加反应的各物质的分子个数比为_____。32g甲烷完全反应制取甲醇的质量为_____g。
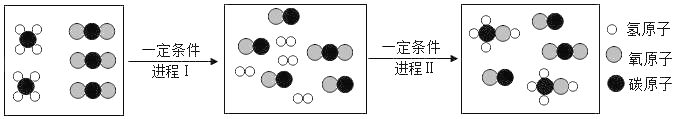
-
科目: 来源: 题型:
查看答案和解析>>【题目】海洋是地球上最大的储水库。蕴含着丰富的化学资源,开发前景十分远大:
(1)目前海水淡化普遍采取的方法是_____。
(2)海水晒盐能够得到粗盐,某兴趣小组同学选取一些粗盐样品,想制得较纯净的精盐,进行如下实验探究:
步骤一:除去泥沙等难溶性杂质、操作的主要步骤为溶解,过滤、_____,在最后一步中玻璃棒的作用为_____;
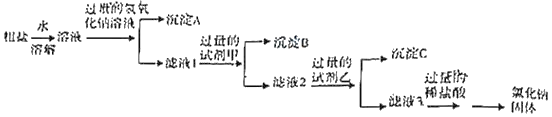
步骤二:除去步骤一所得粗盐中的可溶性杂质氯化镁、氯化钙、碳酸钠,采用如图所示流程:
写岀试剂甲溶液的溶质是_____,沉淀C的成分是_____;(均填化学式)
某同学通过对滤液3成份的检验与分折,确定杂质氯化镁、氯化钙、硫酸钠已被完全去除干净,设计实验方案如下:
实验操作步骤
实验现象
实验结论
步骤一:取少量滤液3于试管中,加入足量_____;过滤,向白色沉淀中加入过量稀硝酸
产生白色沉淀;白色沉淀全部溶解
证明滤液3中含有_____,没有氯化钙和硫酸钠
步骤二:向步骤一反应后所得滤溶液中加入无色酚酞
溶液变红
证明滤液中含有_____,没有氯化镁
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学们在实验室里探究某些酸、碱,盐之间是否发生复分解反应。
(查阅资料)碳酸钾与碳酸钠有相似的化学性质
(实验与探究)
内容
现象
结论
实验一

_____
生成物中有_____或有水或有沉淀生成时复分解反应可以发生
实验二
溶液颜色由红色恰好变为无色
实验三
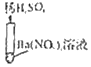
产生白色沉淀
实验结束后某同学把三个实验所得废液倒入同一烧杯中,完全反应后。取少量烧杯中的上层无色清液a的倒入一支洁净的试管中,向清液a中逐滴滴加K2CO3溶液。在滴加过程中,发现先产生气泡,然后又产生白色沉淀、根据上述现现象,请你判断清液a中中的溶质是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】珍珠粉是一种补钙剂,某兴趣小组对珍珠粉的主要成分及其含量展开了一系列探究。
(实验探究一)(1)珍珠粉的主要成分是什么?
实验
实验操作
实验现象
步骤一
取少量样品于试管中,加入足量_____
产生无色气泡
步骤二
将步骤一产生的气体通入澄清石灰水
产生白色沉淀
②写出步骤二中发生反应的化学方程式_____。
(实验结论)珍珠粉的主要成分为碳酸钙。
(实验探究二)测定珍珠粉中碳酸钙的质量分数。(杂质不与稀盐酸反应)
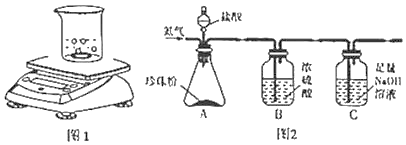
(方案一)(2)该兴趣小组的同学利用如图1所示装置进行实验探究,称得烧杯的质量为40.03g。称得珍珠粉样品的质量为12g。加入足量的稀盐酸质量为200g,完全反应后,电子天平的示数为247.63g。请你计算珍珠粉中碳酸钙的质量分数______。(写出计算步骤:计算结果保留到0.1%)
(方案二)(3)该兴趣小组的同学认为图2所示装置也可测定珍珠粉中碳酸钙的质量分数,需要测定的数据有样品的质量和_____的质量。如果没有装置B,会使测得的碳酸钙的质量分数_____。(填“偏大”、“偏小”或者“不变“)
相关试题

