【题目】根据下列实验装置图,回答有关问题:

(1)实验室常用锌粒和稀硫酸反应制取氢气,若要控制产生氢气的速率,应选择的发生装置是___(从A﹣F中选填字母),写出反应的化学方程式____;
(2)实验室现用G装置制取二氧化碳气体。
①检查装置的气密性:关闭活塞K,将干燥管放入带有水的烧杯中,若观察到____,则表明该装置的气密性良好。
②将装有石灰石的干燥管放入装有稀盐酸的烧杯内,同时打开活塞K,干燥管内发生反应的化学方程式为___,一段时间后,关闭导管上的活塞K,反应停止,其原理是___。该装置的优点是___。
参考答案:
【答案】C; Zn+H2SO4=====ZnSO4+H2↑ 干燥管中液面低于烧杯中液面; CaCO3+2HCl=====CaCl2+H2O+CO2↑; 关闭活塞 K 后,干燥管内由于继续反应生成 CO2 气体,使得装置内气压大于外界大气压, 将干燥管内液体排至烧杯中,使石灰石和稀盐酸完全分离,反应结束 可以控制反应的开始与停止。
【解析】
(1)制取氢气是用锌与稀硫酸反应,反应物的状态是固体和液体,不需要加热,可选用的发生装置是B或C,C中注射器可以控制液体的滴加速度,所以要控制产生氢气的速率,应选择的发生装置是C,锌和稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(2)①检验装置气密性利用装置内外的压强差检验,所以关闭活塞K,将干燥管放入带有水的烧杯中,若观察到干燥管中液面低于烧杯中液面,则表明该装置的气密性良好;
②碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;一段时间后,关闭导管上的活塞K,反应停止,原理是:关闭活塞K后,干燥管内由于继续反应生成CO2气体,使得装置内气压大于外界大气压,将干燥管内液体排至烧杯中,使石灰石和稀盐酸完全分离,反应结束,该装置的优点是:可以控制反应的开始与停止。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示进行有关碳及其氧化物的性质实验(图中固定玻璃管的仪器已略去),下列说法正确的是( )
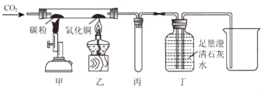
A. 丙装置的作用是收集二氧化碳
B. 该装置的不足之处是未进行尾气处理
C. 甲和乙两处现象分别是黑色粉末减少,黑色粉末逐渐变红
D. 丁装置的作用只是检验乙处发生的反应有二氧化碳生成
-
科目: 来源: 题型:
查看答案和解析>>【题目】向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
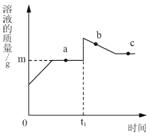
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学是一门以实验为基础的科学。
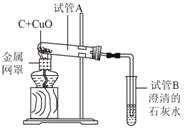
①请写出试管B中发生反应的方程式_____。
②关于实验的下列说法,正确的是_____。
A.金属网罩的作用是集中火焰提高温度
B.若反应前加入的木炭过量,生成的气体还有一氧化碳
C.实验结束后,先熄灭酒精灯,再将导气管移出澄清石灰水
D.实验结束后,试管A中固体减少的质量为氧元素的质量
-
科目: 来源: 题型:
查看答案和解析>>【题目】水和溶液与人们的生活息息相关。
(1)KNO3和NaCl的溶解度曲线如图甲所示。20℃时取18gKNO3和18gNaCl分别放入两只烧杯中,各加入50mL水(水的密度近似看做1g/cm3),充分溶解,现象如图乙所示;升温到50℃时,现象如图丙所示。请回答下列问题:
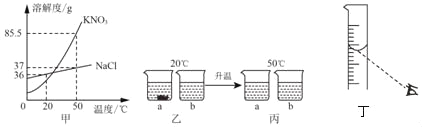
①乙图中,a烧杯溶液中溶质的质量分数____b烧杯溶液中溶质的质量分数(选填“>”、“<”或“=”)。
②要使丙图中的NaCl溶液恰好变成饱和溶液,需要加入____gNaCl固体。
③除去固体KNO3中混有的少量NaCl,实验步骤:先加水加热溶解,再____,然后过滤、洗涤、干燥。
④把溶质质量分数为6%的NaCl溶液稀释成50g质量分数为3%的NaCl溶液,需要水的体积是___mL.若采用图丁所示的操作来量取水的体积(其他操作均正确),则所得溶液的溶质质量分数____(选填“>”、“<”或“=”)3%。
(2)水是一种常用的溶剂,下列各组固体物质能用水鉴别的是____(填字母)。
A.碳酸钙和氯化钠 B.硝酸铵和氯化钠 C.氯化镁和氯化钠 D.氢氧化钠和氯化钠
-
科目: 来源: 题型:
查看答案和解析>>【题目】图中A~H是初中化学常见的物质,且分别由H、C、O、S、Fe、Cu、Ag中一种或几种元素组成。其中A、B、C、G为单质,B为紫红色固体,D、E、F为氧化物,D中两种元素质量之比为4:1,H的水溶液为蓝色。图中“﹣”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
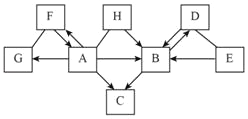
(1)写出化学式:G_____,H_____。
(2)写出D与E反应的化学方程式_____。
(3)写出B→C反应的化学方程式_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】将光亮镁条放入一定量的氯化铵溶液中,发现最终生成灰白色固体[Mgx(OH)yClz]外,还有气体生成。某同学对该现象作如下探究。
(一)生成气体可能是H2、HCl、NH3中的一种或几种。
(查阅资料)
①浓硫酸既可以吸收水,也可吸收氨气;
②常温下,氨气和氯化氢气体反应生成白色固体氯化铵(NH4Cl);
③2NH3+3CuO
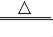 3Cu+N2+3H2O;
3Cu+N2+3H2O;④H2+CuO
 Cu+H2O。
Cu+H2O。(实验探究)收集气体,将气体通过如图装置(各步反应均完全);
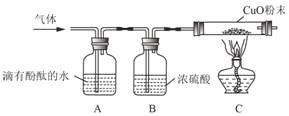
①A装置中出现红色,证明有_____;
②A、B实验装置_____(填“能”或“不能”)对调,理由是_____;
③C中玻璃管内观察到_____,证明有H2。
(反思与评价)他认为不需要单独检验HCl,就能证明HCl不存在,请你评价这种说法是否合理_________并说明理由___________。
(二)过滤、洗涤、一定温度下烘干得灰白色固体。
(查阅资料)灰白色固体Mgx(OH)yClz受热会分解,只生成MgO和HCl。
(实验探究)
取一定量灰白色固体样品,充分加热,得到4g白色固体和3.65g气体。
(结论)
①x:z=_____;
②若所得灰白色固体的相对分子质量为153,则所得灰白色固体的化学式是_____。
(反思与评价)有同学认为不需要任何数据,就可以求出x:z的值,请你说出理由_____。
相关试题

