【题目】如图是A、B、C三种固体物质的溶解度曲线,请回答:
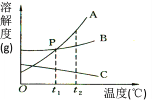
(1)三种物质中,溶解度受温度影响较小的是_____。
(2)t1℃时曲线交点P表示______。
(3)t2℃时A物质的不饱和溶液变成饱和溶液的方法是______。
(4)A物质中混有少量B物质时,可采用_____________的方法得到较纯净的A物质。
(5)t1℃时A、B、C三种物质的饱和溶液同时升温到t2℃,此时溶液中溶质质量分数的大小关系是___________________。
参考答案:
【答案】 B t1℃时A、B两种物质的溶解度相同 增加溶质 降温结晶 A=B>C
【解析】(1)根据溶解度曲线的变化趋势分析解答;
(2)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(3)根据不饱和溶液与饱和溶液相互转化的方法分析解答;
(4)据A、B的溶解度受温度影响情况分析提纯物质的方法;
(5)据三种物质的溶解度随温度变化情况及饱和溶液中溶质质量分数的计算式分析解答。
解:(1)观察溶解度曲线可知,三种物质中,溶解度受温度影响较小的是:B;
(2)t1℃时曲线交点P表示:t1℃时A、B两种物质的溶解度相同;
(3)由于A物质的溶解度随温度的升高而增加且受温度的影响变化较大,所以t2℃时A物质的不饱和溶液变成饱和溶液的方法是:增加溶质;
(4)由于A物质的溶解度随温度的升高而增加且受温度的影响变化较大,当A物质中混有少量B物质时,可采用降温结晶的方法得到较纯净的A物质;
(5)据图可知:A、B的溶解度随温度的升高而增大,C的溶解度随温度的升高而减小;所以将t2℃时A,B,C三种物质的饱和溶液均降温到t1℃时,A、B析出晶体,依然是饱和溶液,又t1℃时A、B的溶解度相同,此时A、B的溶质质量分数相等,而C变为不饱和溶液,溶质的质量分数与降温前相等,据饱和时质量分数的计算式![]() ×100%,可知溶解度越大质量分数也就越大,t1℃时溶液中溶质质量分数的大小关系是:A=B>C。
×100%,可知溶解度越大质量分数也就越大,t1℃时溶液中溶质质量分数的大小关系是:A=B>C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小苏打(碳酸氢钠)在日常生活中有广泛的用途,工业上制取小苏打有多种方法,其中有一种是气相固碳法,其利用的原理是:Na2CO3 + H2O + CO2 =2NaHCO3
资料:碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
温度/℃
0
15
20
30
40
50
60
碳酸氢钠溶解度/g
6.9
8.72
9.6
11.1
12.7
14.45
16.4
碳酸钠溶解度/g
7.1
13.25
21.8
39.7
48.8
47.3
46.4
同学们多次重复实验,所得实验结果基本一致。有同学提出分析第10min时溶液中溶质的组成,于是同学们设计如下实验方案进行实验。
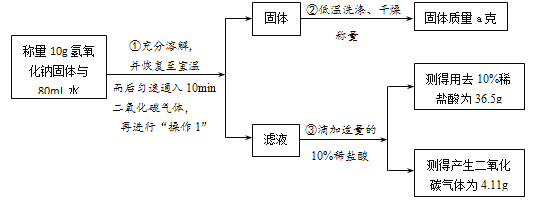
⑴ 实验步骤①中,“操作1”是________,实验步骤③中,为保证测量稀盐酸质量的准确,则应预先进行的实验操作是________;
⑵ 通过数据分析,通入10min二氧化碳时溶液中溶质至少有________;实验中“固体质量a克”,a的最大值是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】图中的①、②分别是钠元素、氯元素在周期表中的信息,A、B、C、D是四种粒子结构示意图。
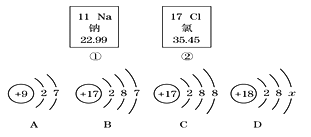
请你回答下列问题:
(1)钠元素的原子序数为______,画出它的原子结构示意图______;氯原子的质子数为 __________。
(2)示意图D中的x =________。
(3)A、B、C、D中属于同种元素的粒子是______和______(填序号)。
(4)A和B两种粒子的______相同,所以它们具有相似的化学性质。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液。它们的转化关系如图所示,回答下列问题。

(1)B的化学式 ,H中溶质的化学式 。
(2)反应③的化学反应方程式为 。
(3)反应①~③中为置换反应的是 (填序号)。
(4)写出稀盐酸与B反应的化学方程式 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质的用途只利用其物理性质的是
A. 硫酸用于金属除锈 B. 熟石灰改良酸性土壤
C. 二氧化碳用于灭火 D. 稀有气体制成电光源
-
科目: 来源: 题型:
查看答案和解析>>【题目】请你根据所学知识并结合下图所示装置回答有关问题:

(1)指出标号仪器的名称:① ;② 。
(2)用高锰酸钾制取氧气的化学方程式为 ,应选择的发生装置是 ,可以用E装置收集氧气的原因是 ,当观察到 现象时,说明氧气已收满;集满氧气的集气瓶应 (填“正”或“倒”)放在桌面上。
(3)制取并收集一定量的二氧化碳,应选择的发生装置是 ,欲制得干燥的二氧化碳,还需将气体通过盛有 (填药品名称)的洗气瓶F。
(4)用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是 ,H中喷有紫色石蕊溶液的纸花显 色。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列粒子结构示意图,回答问题。

(1)上图A、B、C、D四种粒子共表示______种元素。
(2)D原子在化学反应中易___(填“得到”或“失去”)电子。
(3)由B元素和D元素组成的化合物的化学式为______。
(4)E粒子带1个单位正电荷,则X=______。
相关试题

