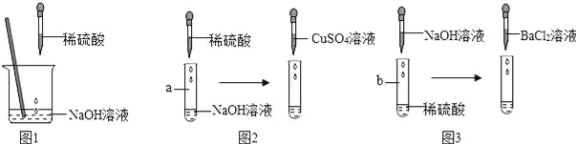
【题目】某兴趣小组以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究。如图1所示,小组同学向烧杯中的氢氧化钠溶液加入稀硫酸,一会儿会发现忘记了滴加指示剂,因此,他们停止滴加稀硫酸,并对烧杯内稀硫酸与氢氧化钠溶液是否发生了反应进行探究。
(1)小组同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH 7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了 |
(2)写出该反应的化学方程式: 。
(3)同学们经过讨论一致认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应,于是分成甲、乙两组继续试验:
甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
【实验操作及现象】如图2,向a试管中滴加足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现蓝色沉淀。
【实验结论】通过以上实验操作及现象,你认为用CuSO4溶液 (填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应。
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应。
【实验操作及现象】如图3,向b试管中滴加足量NaOH溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀。
【实验结论】通过以上实验操作及现象,你认为用BaCl2溶液 (填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应,理由是 。
参考答案:
【答案】(1)<
(2)2NaOH+H2SO4═Na2SO4+2H2O
(3)【实验结论】可以
【实验结论】不可以
稀硫酸、硫酸钠都会电离出硫酸根离子,硫酸根离子都会与钡离子生成硫酸钡沉淀
【解析】试题分析:
(1)硫酸显酸性,溶液的pH值<7,所以
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH<7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
(2)氢氧化钠和稀硫酸反应生成硫酸钠和水,化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
(3)【实验结论】氢氧根离子和铜离子反应会生成氢氧化铜沉淀,所以加入硫酸铜没有蓝色沉淀生成,说明溶液中不含氢氧根离子,可以证明稀硫酸与氢氧化钠溶液能发生反应;
【实验结论】硫酸根离子和钡离子会生成硫酸钡沉淀,用BaCl2溶液不可以证明稀硫酸与氢氧化钠溶液能发生反应,理由是:稀硫酸、硫酸钠都会电离出硫酸根离子,硫酸根离子都会与钡离子生成硫酸钡沉淀。
-
科目: 来源: 题型:
查看答案和解析>>【题目】食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。

①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和 。
②在蒸发过程中,待 时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。

①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是 (用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有 (用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是 。已知:20 ℃时氯化钠的溶解度为36g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2017年4月10日“国际环保环卫展”在北京举行,下列做法不符合环保主题的是
A. 垃圾焚烧 B. 随手关灯 C. 以步代车 D. 废铁回收
-
科目: 来源: 题型:
查看答案和解析>>【题目】在水、铁粉和氦气三种物质中,由原子直接构成的物质是(填化学式) 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三位同学对氯化镁样品(仅含氯化铝杂质)进行如下检测:取457g样品溶于一定量的水中得到8000g溶液,再逐渐加入固体氢氧化钠,反应得到沉淀和加入的氢氧化钠的质量图象如图:(已知氢氧化铝沉淀可以和氢氧化钠溶液反应生成无色溶液,反应方程式为Al(OH)3+NaOH═NaAlO2+2H2O)
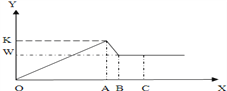
X轴表示加入氢氧化钠的质量,Y轴表示生成沉淀的质量.W为116克,K为272克,试回答下列问题:
(1)如图图象中,A点氢氧化钠的质量为 g,B点氢氧化钠的质量与A点氢氧化钠的质量的差值为 g.
(2)计算氯化镁样品的质量分数(保留到0.01),写出过程.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某研究小组的同学在实验室模拟地震后,灾区居民饮用水处理的过程初步方案如下,请回答下列问题:
(1)在初步对水处理的基础上,将水过滤,除了漏斗、烧杯外,还需要的玻璃仪器是____;其作用是________;若过滤后滤液仍然浑浊,请分析原因_______________________________________________________(任答一条即可).
(2)过滤后常加入明矾,其作用是___________________.
(3)若某同学发现水样呈浅黄色,他净水时可加入____________来脱色.
(4)加入漂白粉或氯气进行消毒杀菌,该步骤发生的是____(填“物理”或“化学”)变化.
(5)将水分发到灾民家中前可用________来检验水的硬度,若要降低水的硬度,可采用最简单的方法是____________.
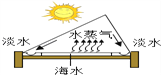
(6)有同学提出了用如图装置进行水处理,请说说你的看法(任答一条即可)__________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某固体由NaOH、Mg(NO3)2、BaC12、K2SO4、CaCO3中的一种或几种组成。加水充分溶解后,有白色沉淀出现,现向该混合物中滴入稀HNO3,沉淀溶解情况如下图所示。下列对该固体组成判断不正确的是
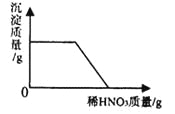
A. 一定含有NaOH B. 可能含有K2SO4
C. 一定含有Mg(NO3)2 D. 可能含有CaCO3
相关试题

