【题目】在其他条件不变的情况下,改变下列条件,一定会同时影响化学反应速率和化学平衡的是
A. 浓度 B. 压强 C. 温度 D. 催化剂
参考答案:
【答案】C
【解析】A、增大固体和纯液体的量,浓度为常数,对反应速率和化学平衡无影响,选项A错误;B、在化学反应前后体积不变的情况下,改变压强对化学平衡无影响,选项B错误;C、所有化学反应都反应热,温度对于任何反应的反应速率和化学平衡都有影响,选项C正确;D、催化剂能改变反应速率,不能使化学平衡移动,选项D错误。答案选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】对于反应4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s) △H= - 444.3kJ/mol,在常温常压下能自发进行,对反应的方向起决定性作用的是
A. 焓变 B. 温度 C. 压强 D. 熵变
-
科目: 来源: 题型:
查看答案和解析>>【题目】印刷电路板在科技领域具有不可替代的作用,它的制备方法为高分子化合物和铜箔压合,通过FeCl3溶液“腐蚀”而成。某实验小组在实验室用废弃的印刷电路板和“腐蚀液”提取铜的一种工艺流程如下:
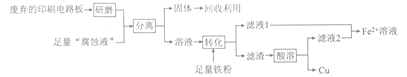
请回答下列问题:
(1) 检验“腐蚀液”中含有Fe2+的方法为_________________。
(2)“分离”所用的操作名称为____________,该操作所用的主要玻璃仪器有烧杯、_____________。
(3)用电解法在铁上镀铜时,阴极材料为_____________(填化学式),理论上电镀过程中电解质溶液的浓度_______________ (填“增大”“减小”或“不变”)。
(4) Fe2+溶液有很多重要用途。
①已知:常温下,Ksp[Fe(OH)2]=1.8×10-16。保存1.8mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊,应调节溶液的pH不超过_________________。
②Fe2+可使Ag+与Fe3+之间相互转化。一定温度下,0.1 mol·L-1的Fe(NO3)2溶液中,c(Fe3+)与c(Ag+)的关系如图所示:
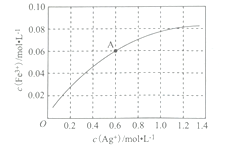
该温度下,A点溶液中转化反应的平衡常数为____________(溶液体积变化忽略不计);若将0.6mol·L-1 Fe(NO3)2溶液、0.15 mol·L-1 Fe(NO3)3溶液、0.06 mol L-1 AgNO3溶液等体积混合后,再加入1.08 g Ag,可观察到的现象为_________________________。
③Fe2+转化为Fe3+后,可用于制备高铁酸盐。向FeCl3溶液中加入NaOH、NaClO溶液制备Na2FeO4的化学方程式为_________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法正确的是( )
A. 离子化合物中只能含离子键,不能有共价键
B. 非金属元素之间形成的化学键一定是共价键
C. 电子数相同的两种微粒一定是同一元素
D. 化学键被破坏的变化不一定是化学变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)
 COS(g)+H2O(g)
COS(g)+H2O(g)实验
温度/K
起始物质的量/mol
平衡物质的量/mol
平衡常数
CO2
H2S
H2O
I
607
0.11
0.41
0.01
II
607
0.22
0.82
III
620
0.1
0.4
6.74×10-3
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质分离(括号内的物质为杂质)的方法错误的是( )
A.硝基苯(苯)--蒸馏
B.乙烯(SO2)--氢氧化钠溶液
C.己烷(己烯)--溴水,分液
D.乙酸乙酯(乙醇)--碳酸钠溶液,分液
-
科目: 来源: 题型:
查看答案和解析>>【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
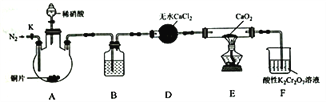
已知:2NO+CaO2 =Ca(NO2)2;2NO2+CaO2=Ca(NO3)2。
请回答下列问题:
(1)将分液漏斗中的稀硝酸滴入三颈烧瓶中的操作为______________。
(2)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因为_________________。
(3)装置D中的仪器名称为_______________。装置B所加试剂为_______________。
(4)装罝F中,酸性K2Cr2O7溶液可将剩余的NO氧化为NO3-,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为_________________。
(5)已知:Ca(NO2)2溶液遇酸会产生NO气体。设计实验证明装置E中有亚硝酸钙生成:____________。
(6)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化空气,又能获得应用广泛的 Ca(NO2)2,反应原理为Ca(OH)2 + NO+NO2=Ca(NO2)2 + H2O。
①若n(NO):n(NO2)>l:l,则会导致______________________________。
②若n(NO):n(NO2)<1:1,则会导致________________________________。
相关试题

