【题目】水合肼 (N2H4·H2O) 常用作还原剂和抗氧剂,其熔点为 -40℃,沸点 118.5℃,极毒。实验室用如下装置制取水合肼(N2H4·H2O)涉及下列反应:

CO(NH2)2+ 2NaOH +NaClO = Na2CO3 + N2H4·H2O + NaCl
N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl]
请回答下列问题:
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)将Cl2通入30%NaOH溶液制备NaClO的化学方程式 。
(3)实验时,如果将 NaOH 和NaClO的混合溶液一次性加入三颈烧瓶,可能会造成的结果是__________。
(4)实验时可根据_________判断N2H4·H2O开始蒸出。
(5)已知:N2H4·H2O + 2I2= N2↑+ 4HI + H2O。测定水合肼的质量分数可采用下列步骤:
①取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液。
②移取10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,加20mL水,摇匀。
③将0.1000mol·L-1碘的标准溶液盛放在__________滴定管中(填“酸式”或“碱式”),当_____________停止滴定,消耗碘的标准溶液为18.00mL,则产品中N2H4·H2O的质量分数为__________。
参考答案:
【答案】
(1)B、D;
(2)Cl2+ 2NaOH=NaClO + NaCl + H2O ;
(3)如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化;
(4)温度计1指示的温度恰为N2H4·H2O的沸点;
(5)酸式;当锥形瓶中溶液由无色变蓝色,且半分钟不褪色;90%
【解析】
试题分析:(1)用天平称量氢氧化钠质量,用量筒量取水的体积,在烧杯中溶解,并用玻璃棒搅拌,所需玻璃仪器除量筒外,还有烧杯、玻璃棒,故答案为:BD;
(2)氯气通入到盛有NaOH的锥形瓶中发生反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O;故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(3)由N2H4H2O+2NaClO=N2↑+3H2O+2NaCl,可知水合肼(N2H4H2O)具有还原性,如果将 NaOH 和 NaClO 的混合溶液一次性加入三颈烧瓶,反应生成的水合肼会被次氯酸钠氧化,故答案为:反应生成的水合肼会被次氯酸钠氧化;
(4)生成水合肼 (N2H4H2O) 进行蒸馏分离,温度计1温度为118.5℃,判断 N2H4H2O 开始蒸出,故答案为:温度计1温度为118.5℃;
(5)碘单质具有氧化性,能腐蚀碱式滴定管的橡胶,则碘水应装在酸式滴定管中;加入最后一滴碘溶液颜色不褪去,溶液呈微黄色且半分钟内不消失,说明滴定到达终点;由N2H4+2I2=N2+4HI,可知250ml溶液中含有的物质的量=0.100mol/L×0.018L×![]() ×
×![]() =0.0225mol,水合肼(N2H4H2O)的质量分数=
=0.0225mol,水合肼(N2H4H2O)的质量分数=![]() ×100%=90%,故答案为:酸式;溶液呈微黄色且半分钟内不消失;90%。
×100%=90%,故答案为:酸式;溶液呈微黄色且半分钟内不消失;90%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在容积不变的密闭容器中进行反应:2SO2 (g)+O2(g)
 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
A. 图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D. 图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
-
科目: 来源: 题型:
查看答案和解析>>【题目】(一)有机化合物
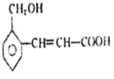 可能发生的化学反应有
可能发生的化学反应有①加成 ②氧化 ③燃烧 ④加聚 ⑤取代
A.①②③ B.①②③④⑤ C.①②③④ D.①③④
(二)已知:A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成食品包装材料。
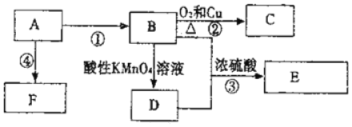
(1)A的结构简式为 。
(2)D分子中的官能团是 。
(3)写出下列反应的化学方程式。
② 。
④ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(一)莽草酸是合成治疗禽流感的药物——达菲的原料之一。莽草酸是A的一种同分异构体,A的结构简式为

回答下列问题:
(1)A的分子式为 。
(2)A可能发生的化学反应有 。(填编号)
①能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②可发生酯化反应
③可与氢氧化钠溶液发生中和反应
④可与金属钠发生置换反应
⑤在铜或银的催化作用下,可被空气中的氧气氧化
(二)乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2g金属钠充分反应,则标准状况下生成气体的体积是 L。
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8g,碱石灰重13.2g。求氧气的的物质的量是 mol,燃烧产物的平均摩尔质量是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)海带中富含碘,请简述检验碘的实验方案_____________________;
(2)已知反应2HI(g)═H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molHI(g)分子中化学键断裂时分别需要吸收436KJ、299KJ的能量,则1molI2(g)分子中化学键断裂时需吸收的能量为_________kJ;
(3)Bodensteins研究了下列反应:2HI(g)
 H2(g)+I2(g)
H2(g)+I2(g)在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
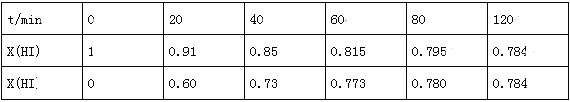
①根据上述实验结果,该反应的平衡常数K的计算式为:______________;(不用求出结果)
②其他条件不变,向平衡后体系中再加入少量HI,则平衡向_______(填“正”或“逆”)反应方向移动,达到平衡后x(HI)_______(填“增大”、“减小”或“不变”)。
③上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为_______(以K和K正表示);若k正=0.0027min-1,在t=40min时,v正=________min-1.
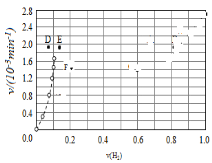
④由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为__________(填字母)。

-
科目: 来源: 题型:
查看答案和解析>>【题目】t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )

A.加热蒸发饱和Ag2CrO4溶液再恢复到t℃,可使溶液由Y点变到Z点
B.在X点没有Ag2CrO4沉淀生成,则此时温度低于t℃
C.向饱和Ag2CrO4溶液中加入少量AgNO3固体,可使溶液由Z点到Y点
D.在t℃时,Ag2CrO4的Ksp为1×10-9
-
科目: 来源: 题型:
查看答案和解析>>【题目】据媒体报道,以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池(PEMFC) 常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是
①正极反应为:O2+4H++4e- ═2H2O
②负极反应为:2H2-4e- ═4H+
③总的化学反应为:2H2+O2
 2H2O
2H2O ④H+通过电解质向正极移动
A.①②③④ B.②③④ C.①②④ D.①②③
相关试题

