【题目】在标准状况下,称量一个充满氯气的容器质量为74.6g,若改充氮气,其质量为66g,则容器的容积为
A.11.2LB.5.6LC.4.48LD.2.24L
参考答案:
【答案】C
【解析】
设容器的质量为m,充满气体时物质的量为n mol,可得71n+m=74.6g,28n+m=66g,两式相减解得n=0.2mol,则容器的容积为:0.2mol×22.4L/mol=4.48L,答案选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】能证明次氯酸是一种弱酸的事实是( )
A.次氯酸不稳定,易分解
B.次氯酸钙可与CO2和H2O反应
C.次氯酸是一种强氧化剂
D.次氯酸能漂白有色纸张
-
科目: 来源: 题型:
查看答案和解析>>【题目】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。

提示:2Fe(OH)3
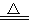 Fe2O3 + 3H2O
Fe2O3 + 3H2O(1)铝在空气中有强的抗腐蚀性,原因是 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为 ________________________。
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,反应完后溶液呈碱性,此反应的离子方程式为
_____________________。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式: 、 。
②产品中AlCl3的质量分数为(只列出计算式,不计算结果) 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某原电池装置如图所示.下列有关叙述中,正确的是( )

A.Fe作正极,发生氧化反应
B.负极反应:2H++2e﹣=H2↑
C.工作一段时间后,两烧杯中溶解pH均不变
D.工作一段时间后,NaCl溶液中c(Cl﹣)增大 -
科目: 来源: 题型:
查看答案和解析>>【题目】I.某火力发电厂以煤为燃料,排出的废气中含有CO2、SO2、水蒸气。为检验该废气中的成分,用如图所示的装置进行实验:

(1)仪器连接的顺序为(填导管接口字母) ;
(2)根据 现象证明有CO2;
(3)装置B的作用是 ,装置D的作用是 。
II. 为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)

(4)亚硫酸钠与浓硫酸反应的化学方程式: ;
(5)为探究干燥的SO2 能不能使品红褪色,请指出设计的实验装置图中两个明显的不足:
① ,
② ;
(6)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是SO2直接导致。所以,SO2 通过品红水溶液后,引起品红褪色的微粒可能是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定条件下,对于反应:CaCO3(块状)+2HCl=CaCl2+CO2↑+H2O,为加快反应速率,下列方法可行的有( )
①增加盐酸的浓度 ②增加同浓度盐酸的用量 ③加水 ④增加CaCO3(块状)的用量 ⑤将块状CaCO3改为粉末状CaCO3
A.1项
B.2项
C.3项
D.4项 -
科目: 来源: 题型:
查看答案和解析>>【题目】下列措施中肯定能使化学反应速率增大的是( )
A.增大反应物的量
B.增大压强
C.升高温度
D.以上措施均可
相关试题

