【题目】关于下列两种物质的说法,正确的是


A. 核磁共振氢谱都有3个吸收峰
B. 都不能发生消去反应
C. 都能与Na反应生成H2
D. 都能在Cu作催化剂时发生氧化反应
参考答案:
【答案】C
【解析】
A. 核磁共振氢谱吸收峰的个数代表有机物分子不同环境的氢原子数;
B. 醇类有机物发生消去反应时,连接羟基的相邻C原子上必须有H原子;
C. 醇与Na反应时,醇羟基上的H原子被钠置换成氢气;
D. 在Cu作催化剂时发生去氢氧化。
A. 根据等效氢思想可知,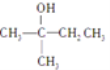 核磁共振氢谱吸收峰有4种,
核磁共振氢谱吸收峰有4种,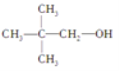 核磁共振氢谱吸收峰有3种,故A项错误;
核磁共振氢谱吸收峰有3种,故A项错误;
B. 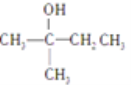 在一定条件下可以发生消去反应生成
在一定条件下可以发生消去反应生成![]() 或者
或者![]() ,而
,而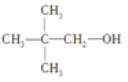 因连接羟基相邻碳原子上无H,则不能发生消去反应,故B项错误;
因连接羟基相邻碳原子上无H,则不能发生消去反应,故B项错误;
C. 醇与Na反应时,醇羟基上的H原子与钠反应生成氢气,两者中均含有羟基,故C项正确;
D. 在Cu作催化剂时,醇会发生氧化反应,断键位置主要是羟基氢原子与连接羟基的碳原子上的氢原子,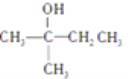 连接羟基的碳原子上无H,故不能发生去氢氧化,
连接羟基的碳原子上无H,故不能发生去氢氧化,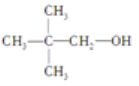 可以被氧化为酮,故D项错误;
可以被氧化为酮,故D项错误;
答案选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知A是一种红棕色金属氧化物,B、D是常见的金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。

(1)写出下列物质的化学名称:A:_________I:_________J:_________G:_________
(2)写出C→I的离子方程式:_____________________________________________________。
(3)写出F→G实验现象:_________________________________________________________。
(4)将一定量A和C混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:

①混合物中含A的质量为______________;
②所用硫酸溶液物质的量浓度为___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项
①
②
③
实验结论
A
浓盐酸
KMnO4
紫色石蕊试液
氯气具有酸性、漂白性
B
浓硫酸
蔗糖
溴水
浓硫酸具有脱水性、氧化性
C
稀硝酸
Na2SO3
品红溶液
实验室制取并检验SO2
D
浓硝酸
Na2CO3
Na2SiO3溶液
非金属性:N>C>Si
A.AB.BC.CD.D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法正确的是
A.
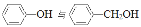 互为同系物
互为同系物B.
 的系统命名是2-甲基-1-丙醇
的系统命名是2-甲基-1-丙醇C. 相同压强下的沸点:乙醇>乙二醇>丙烷
D. 室温下,在水中的溶解度:甘油>苯酚> 1-氯丁烷
-
科目: 来源: 题型:
查看答案和解析>>【题目】钇的常见化合价为+3价,我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
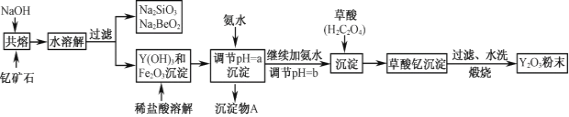
已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
离子
开始沉淀时的pH
完全沉淀时的pH
Fe3+
2.1
3.1
Y3+
6.0
8.2
②在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)写出Na2SiO3的一种用途________________________。
(2)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为__________。
(3)根据元素周期表的知识判断,常温下,氯化锶溶液pH____7(填“大于”、“等于”或“小于”);写出氯化锶的电子式:______________________。
(4)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
① 最好选用盐酸和_______两种试剂,再通过必要的操作即可实现。
A.NaOH溶液 B.氨水 C.CO2 D.HNO3
② 写出Na2BeO2与足量盐酸发生反应的离子方程式___________________________。
(5)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在_________范围内;继续加氨水调节pH =b发生反应的离子方程式为____________________________;检验Fe3+是否沉淀完全的操作方法是:___________________________________。
(6)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式___________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列离子方程式书写正确的是( )
A.向NH4HSO4溶液中加入少量NaOH稀溶液:NH4++OH-=NH3·H2O
B.Cl2通入氢碘酸溶液中:Cl2+2HI=I2+2H++2Cl-
C.向Ca(ClO)2溶液中通入过量SO2:ClO-+SO2+H2O=HClO+HSO3-
D.NO2通入AgNO3溶液中:3NO2+H2O=2NO3-+NO+2H+
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、
 等)中回收碘,实验过程如下:
等)中回收碘,实验过程如下:
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_______;该操作将I2还原为I-的目的是___________________。
(2)操作
 的名称为__________。
的名称为__________。(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是__________________;仪器a的名称为________;仪器b中盛放的溶液为__________。

(4)已知:
 ;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_______________________________________________________________________________;
③另从水层中取少量溶液,加入1-2mL淀粉溶液,加盐酸酸化后,滴加Na2SO3溶液,若溶液变蓝说明废水中含有IO3-;否则说明废水中不含有IO3-。
(5)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含废液回收碘。完成ClO2氧化I-的离子方程式:________________________________。
(6)“碘量法”是一种测定S2-含量的有效方法。立德粉ZnS·BaSO4是一种常用的白色颜料,制备过程中会加入可溶性的BaS,现用“碘量法”来测定立德粉样品中S2-的含量。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol/L 的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的I2用0.1000 mol/L Na2S2O3 滴定,反应式为I2 + 2S2O32-=2I-+ S4O62-。测定消耗Na2S2O3溶液体积V mL。立德粉样品S2-含量为__________(写出表达式)
相关试题

