【题目】下列物质中, 不能使酸性KMnO4溶液褪色的物质是
A.SO2 B. FeSO4 C. 甲烷 D. 乙烯
参考答案:
【答案】C
【解析】
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组多电子原子的能级能量比较不正确的是
①2p=3p ②4s>2s ③4p>4f ④4d>3d
A.①④B.①③C.③④D.②③
-
科目: 来源: 题型:
查看答案和解析>>【题目】按要求填空
(1)已知实验室制备氧气可以通过加热高锰酸钾实现,其发生的反应如下:2KMnO4 K2MnO4+MnO2+O2↑其中被氧化的元素是 , 还原产物是 .
K2MnO4+MnO2+O2↑其中被氧化的元素是 , 还原产物是 .
(2)查阅资料可知:铜和浓H2SO4共热,发生如下反应:Cu+2H2SO4 CuSO4+SO2↑+2H2O该反应中氧化剂与还原剂的物质的量之比为 , 其中H2SO4在反应中体现性.
CuSO4+SO2↑+2H2O该反应中氧化剂与还原剂的物质的量之比为 , 其中H2SO4在反应中体现性.
(3)在一定条件下,RO3n﹣和氟气可发生如下反应:RO3n﹣+F2+2OH﹣=RO4﹣+2F﹣+H2O从而可知在RO3n﹣中元素R的化合价是 .
(4)请用双线桥表示下列反应方程式中转移的电子数目及方向:
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
若反应中,发生氧化反应的HCl为1.2mol,则被还原的K2Cr2O7物质的量为 mol. -
科目: 来源: 题型:
查看答案和解析>>【题目】以白云石(化学式表示为MgCO3·CaCO3)为原料制备氢氧化镁的工艺流程如下:
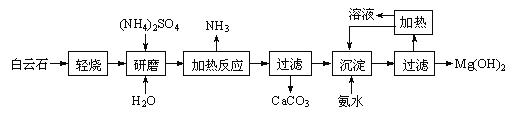
已知:①白云石加热过程中,固体失重百分比与温度的关系如下图所示:

② Ksp[Mg(OH)2]=5.61×10-12。
(1)根据流程图判断白云石“轻烧”后固体产物的主要成份 _____(填化学式)。结合上图判断“轻烧”温度应不超过 _____。
(2)“加热反应”的化学方程式为_________________________。
(3)沉淀过程溶液的pH=9.5,此时溶液中c(Mg2+)= _______(已知)。
(4)该工艺中可以循环使用的物质是________(填化学式)。
(5)传统工艺将白云石分解为氧化镁和氧化钙后提取,从环境保护的用度分析,该工艺采用轻烧白云石的方法,其优点是__________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL.一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
(1)配制溶液时,其正确的操作顺序为(填序号).本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、、 .
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状态如图所示.烧杯的实际质量为g,要完成本实验该同学应称量g NaOH.
(3)使用容量瓶前必须进行的一步操作是 .
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是(填序号).
A.转移溶液时,有少量溶液洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却至室温就将溶液移入容量瓶中并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线. -
科目: 来源: 题型:
查看答案和解析>>【题目】苹果酯是一种具有新鲜青苹果香味的日用香精,其合成线路如下图所示部分 产物已略去):

己知:i: 2mol F在一定条件下生成lmol G和lmol乙醇
ii:羰基化合物(醛或酮)与醇在一定条件下可以生成醚,如:

回答下列问题:
(1)F的分子式为 _________, 其名称为_________。
(2)A→B的化学方程式为______ ,其反应类型为__________。
(3)足量D与H反应的化学方程式为______________. 其反应类型为__________。
(4)N为F的酯类同分异构体,且能发生银镜反应,则N的结构简式可能为:__________。
(5)请以氯化苄(
 )和H为起始原料,选用必要的无机试剂合成苯甲醛乙二醇缩醛(
)和H为起始原料,选用必要的无机试剂合成苯甲醛乙二醇缩醛( ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________ -
科目: 来源: 题型:
查看答案和解析>>【题目】超细氧化镍(NiO)是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以Ni(NO3) 6H2O和[CO(NH2)2](尿素)为原料制备。
(1)Ni2+基态核外电子排布式为_____________。
(2)与NO3-离子互为等电子体的一种分子的分子式为__________。
(3)尿素分子中碳原子轨道的杂化类型为________,1mol尿素分子中含有的σ键的数目为______。
(4)C、N、O三种元素第一电离能由大到小的顺序为_________。
(5)NiO(氧化镍)晶体的结构与NaCl相同,但天然的和绝大部分人工制备体都存在各种缺陷,例如在某种NiO晶体中就存在如右图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。经测定某氧化镍样品中Ni3+与Ni2+的离子数之比为6:91,若该晶体的化学式为NixO,则x=________。

相关试题

