【题目】下列反应的离子方程式书写正确的是
A. 铜溶于0.5mo/L的硝酸:Cu+4H++2NO3- =Cu2++2NO2↑+2H2O
B. Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
C. 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D. Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
参考答案:
【答案】D
【解析】铜溶于0.5mo/L的硝酸生成NO,离子方程式是3Cu+8H++2NO3- =3Cu2++2NO↑+4H2O,故A错误;Na2S2O3溶液中加入稀硫酸,+2价S发生歧化反应2生成S单质、SO2气体,反应离子方程式是S2O32-+2H+═SO2↑+S↓+H2O,故B错误;向Ba(OH)2溶液中加入少量的NH4HSO4溶液,反应离子方程式是Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+H2O+ ![]() ,故C错误;Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙、碳酸氢钠、水,反应离子方程式是:HCO3-+Ca2++OH-=CaCO3↓+H2O,故D正确。
,故C错误;Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙、碳酸氢钠、水,反应离子方程式是:HCO3-+Ca2++OH-=CaCO3↓+H2O,故D正确。
-
科目: 来源: 题型:
查看答案和解析>>【题目】胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量;1 mol CH4 完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写中正确的是( )
A. CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=890.3 kJ·mol-1
B. CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-890.3 kJ·mol-1
C. CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-890.3 kJ
D. 2H2(g)+O2(g)===2H2O(l)ΔH=-517.6 kJ
-
科目: 来源: 题型:
查看答案和解析>>【题目】对常温下
 的
的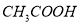 溶液,下列叙述不正确的是
溶液,下列叙述不正确的是A.
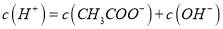
B. 加入少量
 固体后,
固体后, 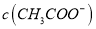 降低
降低C. 该溶液中由
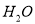 电离出的
电离出的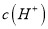 是
是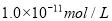
D. 与等体积
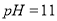 的
的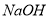 溶液混合后所得溶液显酸性
溶液混合后所得溶液显酸性 -
科目: 来源: 题型:
查看答案和解析>>【题目】氨气有广泛用途,工业上利用反应N2(g)+3H2(g)
 2NH3(g) H<0合成氨,其基本合成过程如下:
2NH3(g) H<0合成氨,其基本合成过程如下: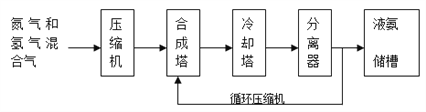
(1)某小组为了探究外界条件对反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
①a条件下,0~t0的平均反应速率v(N2)=___________mol·L-1·min-1。
②相对a而言,b可能改变的条件是______________________________。
③在a条件下t1时刻将容器体积压缩至原来的1/2,t2时刻重新建立平衡状态。请在答题卡相应位置画出t1~t2时刻c(H2)的变化曲线________。
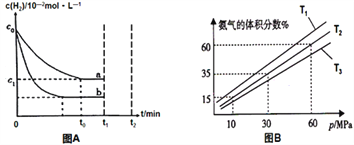
(2)某小组往一恒温恒压容器充入9 mol N2和23 mol H2模拟合成氨反应,图B为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
① 此时N2的平衡分压为__________MPa,H2的平衡分压为___________MPa。(分压=总压×物质的量分数)
② 列式计算此时的平衡常数Kp=____。(用平衡分压代替平衡浓度计算,结果保留2位有效数字)
(3)分离器中的过程对整个工业合成氨的意义是_____________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某无色透明的溶液中加入金属锌有H2放出,则在该溶液中一定能大量共存的是( )
A.Cu2+ Cl﹣ K+ SO42﹣
B.Na+ NO3﹣ OH ﹣ CO32﹣
C.Ba2+ Cl﹣ NO3﹣ SO42﹣
D.K+ Na+ Cl﹣ SO42﹣ -
科目: 来源: 题型:
查看答案和解析>>【题目】牙齿洁白,人人喜欢。将漂白剂沾在牙套上,牙齿咬住牙套可使牙齿变得洁白。下列物质溶于水后所得溶液可作为牙齿漂白剂的是
A.Cl2 B.HNO3 C.Na2O2 D.H2O2
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列解释事实的离子方程式不正确的是
A. 铝片放入NaOH 溶液中有气体产生: 2Al+ 2OH-+ 2H2O=2AlO2-+3H2↑
B. 向K2Cr2O7溶液中滴加少量浓H2SO4,溶液橙色加深:Cr2O72-(橙色)+ H2O
 2CrO42-(黄色) + 2H+
2CrO42-(黄色) + 2H+C. 用Na2CO3溶液浸泡锅炉水垢(含CaSO4):CaSO4 + CO32-
 CaCO3+ SO42-
CaCO3+ SO42-D. 向Na2SiO3溶液中通入过量CO2制各硅酸凝胶:SiO32-+ CO2 + H2O=H2SiO3(胶体) + CO32-
相关试题

