【题目】一定条件下,物质的量均为0.3mol的X(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g) ![]() 2Z(g),ΔH=-akJ/mol,下列说法正确的是
2Z(g),ΔH=-akJ/mol,下列说法正确的是
A. 反应一段时间后,X与Y的物质的量之比仍为1:1
B. 达到平衡时,反应放出0.1akJ的热量
C. 达到平衡后,若向平衡体系中充入稀有气体,Z的正反应速率将不发生变化
D. X的体积分数保持不变,说明反应已达到平衡
参考答案:
【答案】CD
【解析】A.Y的起始量未知,X、Y以1:3转化,则不能确定反应一段时间后X、Y的物质的量关系,故A错误;B.物质的量与热量成正比,且参加反应的X的物质的量未知,不能计算达到平衡时放出的热量,故B错误;C.容积固定的密闭容器,充入稀有气体,X、Y、Z的浓度不变,则反应速率不变,平衡不移动,故C正确;D.该反应为气体体积减小的反应,体积分数不变,说明反应已达到平衡,故D正确;故选CD。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu

(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是___________
②Cu电极上发生的电极反应式为__________
③原电池工作时,盐桥中的_____离子(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是______极;
②图丙中的②线是_________离子的变化。
③当电子转移为2mol时,向乙烧杯中加入_____L5mol/LNaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O
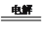 Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________
Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为___________
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
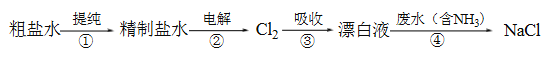
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了探究过氧化钠的强氧化性,某小组设计了如图所示的实验装置。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接仪器。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待产生连续气泡后,将装置D中的导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N2,直至装置中气体变为无色。
回答下列问题:
(1)装置D中收集的无色气体能使带火星的木条复燃,据此推断该气体是_______,解释产生该气体的原因是(用化学方程式表示)____________________________。
(2)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学根据A中气体的颜色推测试纸变蓝时发生的反应可能是(写离子方程式)____________________________;乙同学认为使试纸变蓝的原因也可能是____________________________。
(3)资料显示,Na2O2与干燥的HCl能发生化学反应生成Cl2,该反应的化学方程式为:_________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。

(1)装置A制取氯气,该反应的化学方程式:___________。
(2)装置C中发生复分解反应制取SO2,该反应的化学方程式:___________。
(3)为验证SO2和Cl2发生了反应,小组同学又继续如下实验。
①甲同学认为若SO2和Cl2反应,生成了Cl-,只要检验到生成的Cl-即可,甲取适量B中样品于试管中,向其中滴加少量___________溶液,有白色沉淀生成。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得到正确结论。洗气瓶中盛有试剂的名称是___________。
③丙同学认为按乙同学的建议改进实验也不合理,理由是:___________。
④丙同学取溶液X于试管中,加入少量反应后B中的溶液,生成大量白色沉淀,得出正确结论:SO2与Cl2同时通入水中,可以发生反应。溶液X是_________(填选项序号)。
a. BaCl2溶液 b. Ba(OH)2溶液 c. 氯水 d. 石蕊溶液
SO2与Cl2同时通入水中反应的化学方程式是______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】四种短周期主族元素 X、Y、Z、W 的相对位置如表,元素 X 的原子核外电子数是 Z的 2 倍。下列说法不正确的是
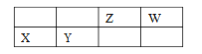
A. W 元素的简单气态氢化物的热稳定性比 Z 元素的简 单气态氢化物的高
B. 气体分子(ZW)2 的结构式为 N≡C—C≡N
C. X、Y、W 三种元素的简单离子半径最大的是 Y
D. 元素 X 位于周期表中第三周期、第ⅡA族,其单质制备可用电解熔融 XCl2 的方法。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,相关物质间的关系如下图所示。

(1)H的化学式是______________。
(2)反应①的化学方程式是____________________________。
(3)反应②的离子方程式是____________________________。
(4)检验F溶液中金属阳离子的操作和现象是____________________________。
(5)H转化为G的实验现象是__________________________________________。
(6)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是_______(填下图字母)

相关试题

