【题目】下列物质均为常见物质或它们的溶液,其中A为淡黄色固体,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱。根据它们之间的转化关系(下图), 用化学用语回答问题。(部分产物已省略)
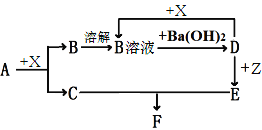
(1)写出下列物质的化学式:A______,B_______D_______。
(2)A与SO3(g)的反应类似于A与X的反应,请写出A与S03(g)反应的化学方程式_______。
(3)向Z溶液中通入一定量的Cl2,写出检验Z中阳离子是否反应充全所需试剂:______。
(4)物质E转化为物质F的现象为_____, 化学方程式为______。
参考答案:
【答案】 Na2O2 Na2CO3 NaOH 2SO3+2Na2O2==2Na2SO4+O2 K3Fe(CN)6(或KMnO4溶液) 白色沉淀转化为灰绿色沉淀,最终转化为红褐色沉淀 4Fe(OH)2+2H2O+O2=4Fe(OH)3
【解析】根据题意可知:A为淡黄色固体,是过氧化钠;Z为浅绿色溶液,含有亚铁离子溶液;D为一种常见的强碱,是氢氧化钠;能够与过氧化钠反应生成无色气体的无色气体是二氧化碳,生成的无色气体为氧气;碳酸钠与氢氧化钡溶液反应生成氢氧化钠;
(1)通过以上分析可知:A是Na2O2,B是Na2CO3, D是NaOH;正确答案:Na2O2;Na2CO3; NaOH。
(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气,过氧化钠与SO3(g)的反应生成硫酸钠和氧气,化学方程式为:2SO3+2Na2O2==2Na2SO4+O2 ;正确答案:2SO3+2Na2O2==2Na2SO4+O2。
(3)Z溶液中含有亚铁离子,通入氯气后,生成铁离子,要检验Z溶液中亚铁离子是否存在,可以用K3Fe(CN)6(或KMnO4溶液),若没有蓝色沉淀生成或溶液褪色现象,说明亚铁离子已经完全被氧化成铁离子;正确答案:K3Fe(CN)6(或KMnO4溶液)。
(4)OH- 与Fe2+反应生成Fe(OH)2白色沉淀,在有氧气的存在下,白色沉淀被氧化为灰绿色,最终变为红褐色Fe(OH)3;化学方程式:4Fe(OH)2+2H2O+O2=4Fe(OH)3;正确答案:4Fe(OH)2+2H2O+O2=4Fe(OH)3。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列措施中肯定能使化学反应速率增大的是( )
A.增大反应物的量
B.增大压强
C.升高温度
D.以上措施均可 -
科目: 来源: 题型:
查看答案和解析>>【题目】在25℃时;用石墨电极电解 CuSO4溶液(假设溶液的体积在电解前后不发生变化).5min后,在一个石墨电极上有6.4g Cu生成.下列说法中正确的是( )
A.有Cu生成的一极是阴极,发生氧化反应
B.反应中转移电子的物质的量为0.4 mol
C.在另一极得到O2的体积(标准状况)是1.12 L
D.电解一段时间后,溶液的pH不变 -
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氢 ⑥氯酸钾
A. 碱:①④ B. 纯净物:③④⑤ C. 盐:①⑥ D. 混合物:②⑤
-
科目: 来源: 题型:
查看答案和解析>>【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列离子方程式正确的是( )
A. 碳酸氢钠溶液与少量澄清石灰水反应:HC
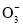 +Ca2++OH-CaCO3↓+H2O
+Ca2++OH-CaCO3↓+H2OB. 氯化铵与氢氧化钠两种溶液混合加热:N
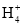 +OH-
+OH- H2O+NH3↑
H2O+NH3↑C. 钠和冷水反应:Na+2H2ONa++2OH-+H2↑
D. 向氯化铝溶液中滴加过量氨水:Al3++3OH-Al(OH)3↓
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜。下列说法中正确的是

A. 铜电极应与X相连接
B. H+经过质子交换膜由右向左移动
C. 当N电极消耗0. 25 mol气体时,则铁电极增重16 g
D. M电极反应式:CO(NH2)2+H2O-6e- =CO2↑+N2↑+6H+
相关试题

