【题目】高温下,某反应平衡常数K= ![]() .恒容条件下达到平衡时,温度升高H2浓度减小.下列说法正确的是( )
.恒容条件下达到平衡时,温度升高H2浓度减小.下列说法正确的是( )
A.该反应的化学方程式为CO+H2O ![]() CO2+H2
CO2+H2
B.该反应的焓变为正值
C.恒温恒容下,增大压强,H2浓度一定减小
D.升高温度,平衡右移,逆反应速率减小
参考答案:
【答案】B
【解析】A.由平衡常数K= ![]() ,可知该反应的化学方程式CO2(g)+H2(g)CO(g)+H2O(g),A不符合题意;
,可知该反应的化学方程式CO2(g)+H2(g)CO(g)+H2O(g),A不符合题意;
B.温度升高时H2浓度减小,说明在升温时平衡正向移动,△H>0,B符合题意;
C.恒容增大压强的方式不确定,所以H2的浓度变化不确定,C不符合题意;
D.升高温度,平衡右移,但v正和v逆都增大,D不符合题意;
所以答案是:B
【考点精析】认真审题,首先需要了解化学平衡常数的含义(指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态),还要掌握化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效))的相关知识才是答题的关键.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
-
科目: 来源: 题型:
查看答案和解析>>【题目】在一定温度下将1molCO 和3mol 水蒸气放在密闭的容器中发生下列反应CO(g)+H2O(g)CO2(g)+H2(g)达到平衡后,测得CO2为0.75mol,再通入6mol 水蒸气,达到新的平衡后,CO2和H2的物质的量之和为( )
A.1.2 mol
B.1.5 mol
C.1.8 mol
D.2.1 mol -
科目: 来源: 题型:
查看答案和解析>>【题目】已知反应A+B
 C+D的能量变化如图所示,下列说法正确的是
C+D的能量变化如图所示,下列说法正确的是
A. 产物C的能量高于反应物的总能量
B. 若该反应中有电子得失,则可设计成原电池
C. 反应物的总能量低于生成物的总能量
D. 该反应中的反应物A和B的转化率定相同
-
科目: 来源: 题型:
查看答案和解析>>【题目】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示【已知:P[c(A-)/c(HA)]=-1g[c(A-)/c(HA)]】。下列叙述不正确的是
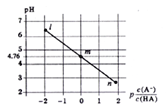
A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液过程中,c(A-)/[c(HA)×c(OH-)]保持不变
C. m点所示溶液中:c(H+)=c(HA)+c(OH-)-c(Na+)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
-
科目: 来源: 题型:
查看答案和解析>>【题目】将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)NH3(g)+HI(g);②2HI(g)H2(g)+I2(g).达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为( )
A.9
B.16
C.20
D.25 -
科目: 来源: 题型:
查看答案和解析>>【题目】具有漂白作用的物质有:①84 消毒液 ②二氧化硫 ③过氧化氢 ④漂白粉,其漂白原理相同的是
A.①③B.②③C.①③④D.①②④
相关试题

