【题目】为了探究某固体化合物X(仅含3种元素,相对分子质量小于200)的组成和性质,设计并完成如下实验,其中X、A、B、C、D均为常见化合物。

请回答:
(1)黄色溶液中的金属阳离子是________。
(2)固体A→白色沉淀B的离子方程式是______________________________。
(3)X的化学式是_____________________________________。
参考答案:
【答案】Fe3+ SO3+Ba2++ H2O=BaSO4↓+2H+ FeSO4
【解析】
由黄色溶液中加入KSCN溶液,溶液变为血红色可知,黄色溶液为氯化铁溶液,则D为氧化铁;由气体C能使品红溶液褪色可知,C为二氧化硫,固体A与氯化钡溶液反应生成白色沉淀B,说明A为三氧化硫、B为硫酸钡;由质量守恒定律可知m(A)=30.4g-
(16.0g+0.1mol×64g/mol)=8.0g,则n(Fe2O3)= 0.1mol ,n(SO2)= 0.1mol ,n(SO3)=0.1mol,由铁原子、氧原子和硫原子个数守恒可知X中n(Fe):n(S):n(O)=0.2:0.2:(0.3+0.2+0.3)
=1:1:4,X为硫酸亚铁。
(1)黄色溶液为氯化铁溶液,溶液中的金属阳离子是Fe3+,故答案为:Fe3+;
(2)固体A→白色沉淀B的反应为三氧化硫与氯化钡溶液反应生成硫酸钡白色沉淀,反应的离子方程式是SO3+Ba2++ H2O=BaSO4↓+2H+,故答案为:SO3+Ba2++ H2O=BaSO4↓+2H+;
(3)由质量守恒定律可知m(A)=30.4g-(16.0g+0.1mol×64g/mol)=8.0g,则n(Fe2O3)= 0.1mol ,n(SO2)= 0.1mol ,n(SO3)=0.1mol,由铁原子、氧原子和硫原子个数守恒可知X中n(Fe):n(S):n(O)=0.2:0.2:(0.3+0.2+0.3)=1:1:4,X为硫酸亚铁,故答案为:FeSO4。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知:X为具有浓郁香味、不易溶于水的油状液体,食醋中约含有3%-5%的D,其转化关系如下图所示。
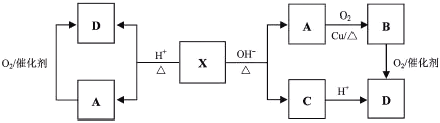
请回答:
(1)X的结构简式是__________________。
(2)A→B的化学方程式是____________________________________________。
(3)下列说法不正确的是________。
A.A+D→X的反应属于取代反应
B.除去X中少量D杂质可用饱和Na2CO3溶液
C.A与金属钠反应比水与金属钠反应要剧烈得多
D.等物质的量的A、B、D完全燃烧消耗O2的量依次减小
-
科目: 来源: 题型:
查看答案和解析>>【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )

A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述正确的是

A.Mg(s)所具有的能量高于MgX2(s)所具有的能量
B.MgCl2电解制Mg(s)和Cl2(g)是吸热过程
C.热稳定性:MgI2>MgBr2>MgCl2>MgF2
D.常温下氧化性:F2<Cl2<Br2<I2
-
科目: 来源: 题型:
查看答案和解析>>【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 0.1 molL﹣1的KI溶液:Na+、Ag+、NO3﹣、SO42﹣
B. 使甲基橙变红色的溶液:NH4+、Cu2+、ClO﹣、Cl﹣
C. c(OH﹣)=0.1mol/L的溶液:Na+、K+、CO32﹣、ClO﹣
D. 0.1 molL﹣1的KMnO4溶液:Na+、K+、Cl﹣、SO32﹣
-
科目: 来源: 题型:
查看答案和解析>>【题目】水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+2H2O,下列说法中不正确的是
A. 每生成1mol Fe3O4,反应转移的电子总数为4mol
B. Fe2+和S2O32﹣都是还原剂
C. x=4
D. 1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
 mol
mol -
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组利用下列装置,进行与氯气相关的实验。
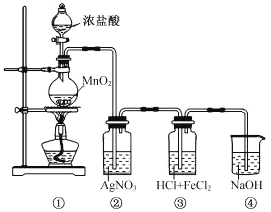
(1)装置④中NaOH溶液的作用是___________。
(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到FeCl3·6H2O晶体。在蒸发浓缩操作中,不需要的仪器是___________。
A.蒸发皿 B.漏斗 C.玻璃棒 D.酒精灯
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2___________________,请说明理由_______________________________________。
相关试题

