2025年天星教育试题调研化学第10辑
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天星教育试题调研化学第10辑 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第74页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
调研
[河南开封 3 月联考]钼(Mo)广泛应用于化工生产、医疗卫生等领域。一种从废催化剂(主要含 NiO、MoO₃、Fe₂O₃、Al₂O₃)中富集回收钼和镍的工艺流程如图所示。
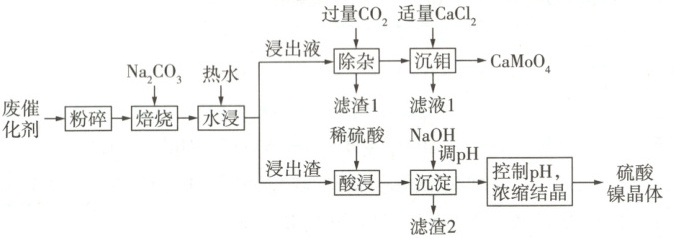
已知:①NiO、Fe₂O₃在高温时均不与 Na₂CO₃反应。②25℃时,$ K_{sp}[Fe(OH)_3] = 2.8×10^{-39} $,$ K_{sp}[Ni(OH)_2] = 2×10^{-16} $,$ K_{sp}(CaMoO_4) = 1.46×10^{-8} $,$ K_{sp}(CaCO_3) = 3.36×10^{-9} $;$ H_2CO_3 $的 $ K_{a1} = 4.5×10^{-7} $,$ K_{a2} = 4.7×10^{-11} $。
(1)“粉碎”废催化剂的目的是
(2)“焙烧”中,废催化剂中的 MoO₃与 Na₂CO₃反应生成可溶性钠盐 Na₂MoO₄,该反应的化学方程式为
(3)“除杂”中,加入过量 CO₂,发生反应的离子方程式为
(4)滤渣 2 的成分是
(5)“沉钼”中,溶液 pH 为 7.0,若条件控制不当,会产生 CaCO₃沉淀。为避免 CaMoO₄中混入 CaCO₃,当溶液中$ \dfrac{c(HCO_3^-)}{c(MoO_4^{2-})} = $
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其作用是
[河南开封 3 月联考]钼(Mo)广泛应用于化工生产、医疗卫生等领域。一种从废催化剂(主要含 NiO、MoO₃、Fe₂O₃、Al₂O₃)中富集回收钼和镍的工艺流程如图所示。

已知:①NiO、Fe₂O₃在高温时均不与 Na₂CO₃反应。②25℃时,$ K_{sp}[Fe(OH)_3] = 2.8×10^{-39} $,$ K_{sp}[Ni(OH)_2] = 2×10^{-16} $,$ K_{sp}(CaMoO_4) = 1.46×10^{-8} $,$ K_{sp}(CaCO_3) = 3.36×10^{-9} $;$ H_2CO_3 $的 $ K_{a1} = 4.5×10^{-7} $,$ K_{a2} = 4.7×10^{-11} $。
(1)“粉碎”废催化剂的目的是
增大反应物接触面积,加快反应速率,提高浸出率
。(2)“焙烧”中,废催化剂中的 MoO₃与 Na₂CO₃反应生成可溶性钠盐 Na₂MoO₄,该反应的化学方程式为
$MoO_3 + Na_2CO_3 \stackrel{焙烧}{=\!=\!=} Na_2MoO_4 + CO_2↑$
。(3)“除杂”中,加入过量 CO₂,发生反应的离子方程式为
$[Al(OH)_4]^- + CO_2 \stackrel{}{=\!=\!=} Al(OH)_3↓ + HCO_3^-$
。(4)滤渣 2 的成分是
Fe(OH)₃
(填化学式)。“沉淀”时,若溶液中金属阳离子的浓度均为 0.02 mol·L⁻¹,应控制溶液 pH 不超过7
。(5)“沉钼”中,溶液 pH 为 7.0,若条件控制不当,会产生 CaCO₃沉淀。为避免 CaMoO₄中混入 CaCO₃,当溶液中$ \dfrac{c(HCO_3^-)}{c(MoO_4^{2-})} = $
$\frac{10^{-7}×3.36×10^{-9}}{4.7×10^{-11}×1.46×10^{-8}}$
(列出计算式)时,应停止加入 CaCl₂溶液。(6)将分离出硫酸镍晶体后的母液收集、循环使用,其作用是
提高镍的回收率
。
答案:
(1)增大反应物接触面积,加快反应速率,提高浸出率
(2)$MoO_3 + Na_2CO_3 \stackrel{焙烧}{=\!=\!=} Na_2MoO_4 + CO_2↑$
(3)$[Al(OH)_4]^- + CO_2 \stackrel{}{=\!=\!=} Al(OH)_3↓ + HCO_3^-$
(4)Fe(OH)₃;7
(5)$\frac{10^{-7}×3.36×10^{-9}}{4.7×10^{-11}×1.46×10^{-8}}$
(6)提高镍的回收率
(1)增大反应物接触面积,加快反应速率,提高浸出率
(2)$MoO_3 + Na_2CO_3 \stackrel{焙烧}{=\!=\!=} Na_2MoO_4 + CO_2↑$
(3)$[Al(OH)_4]^- + CO_2 \stackrel{}{=\!=\!=} Al(OH)_3↓ + HCO_3^-$
(4)Fe(OH)₃;7
(5)$\frac{10^{-7}×3.36×10^{-9}}{4.7×10^{-11}×1.46×10^{-8}}$
(6)提高镍的回收率
查看更多完整答案,请扫码查看


