【题目】化学兴趣小组的同学想对金属活动性的规律以及应用等方面进行探究总结。
实验室中有下列化学药品:铁、铜、锌、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶液和所需要的化学仪器。请按要求完成下面的实验内容:
(1)为了证明Zn、Fe、Cu的活动性顺序,可供选择的试剂种类最少的组合可能为_______。
(2)将等质量的铁和锌分别加入质量分数相同、等质量的稀硫酸中,其反应过程如图所示。 试回答:
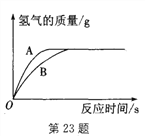
①曲线A表示的是_______(填“铁”或“锌”)跟稀硫酸反应的情况。
②上述曲线图除①能说明的结论外,还可得出的结论有:
a.生成氢气的质量相同;
b.___________________________________________。
参考答案:
【答案】 Zn、FeSO4溶液、Cu(或ZnSO4溶液、Fe、CuSO4溶液) 锌 H2SO4完全反应(合理答案均可)
【解析】(1)锌、铁、铜三种金属的活动性顺序是锌>铁>铜,在比较三种金属的活动性时,常用“三取中”的方法,即取中间金属的盐溶液与两边的金属反应来比较金属的活动性.根据题中的试剂,可用Zn、FeSO4溶液、Cu或ZnSO4溶液、Fe、CuSO4溶液即可;
(2)①由题中曲线,曲线A表示的金属与酸反应速度快,即金属活动性强;锌的活动性比铁强;所以曲线A表示金属锌与酸反应情况;
②由反应过程图可知,生成的氢气的质量相等,参加反应的硫酸的质量相等,反应结束后稀硫酸都没有剩余,铁一定有剩余。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
(1)已知氮化镁中氮元素的化合价为-3价,请你写出生成氮化镁的化学反应式 。
(2)写出镁与二氧化碳反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH
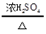 CO↑+H2O。下图是制备干燥的一氧化碳还原氧化铁并检验反应产物的实验装置。
CO↑+H2O。下图是制备干燥的一氧化碳还原氧化铁并检验反应产物的实验装置。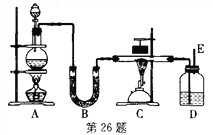
(1)为顺利、安全地完成实验,实验开始时既要检查装置的气密性,还应检验__________,以防爆炸。
(2)装置B中盛放_______,作用是___________。
(3)装置D中盛放_______,检验___________。
(4)写出装置C中反应的化学方程式:___________________。
(5)实验开始时,应先点燃_______(填“A处酒精灯”或“C处酒精喷灯”,下同),实验结束时应先停止_______的加热;E处的作用是___________。
(6)反应后,将磁铁悬在玻璃管上方,其作用是____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学为了体验工业冶炼金属的过程,在实验室里做了用CO还原CuO的实验。他们称得装有CuO粉末的玻璃管重42 g,反应完全后,恢复到室温称量,玻璃管和固体残留物共重40.4 g,并收集到CO2 4.4 g,请你和他们一起计算:
(1) 42 g-40.4 g=l.6 g,1.6 g表示__________________的质量。
(2)该反应制得的铜的质量为__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小丁通过学习知道,电解水时生成氢气、氧气的体积比为2:1,但他在实验开始时发现氢气和氧气的体积比略大于2:1。你认为该现象的合理解释是 ( )
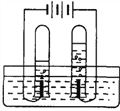
A. 要敢于质疑书本知识,书上的数据本来就是错的
B. 氧气比氢气更易溶于水
C. 生成的氧气有一部分跑到了试管外
D. 氧气的密度比氢气大得多,更难从水中升到水面上
-
科目: 来源: 题型:
查看答案和解析>>【题目】二氧化硫气体是造成酸雨的主要物质。为了探究二氧化硫能与水反应生成具有酸性的物质,四位同学设计了如下一组实验:取几朵用石蕊试液染成紫色的干燥的纸花,按下图进行实验,观察纸花颜色的变化。下列有关的说法,你认为正确的是
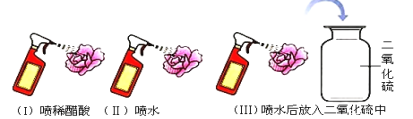
A.小雨同学认为:实验Ⅰ中喷稀醋酸紫色小花变红,是为了证明酸性物质使紫色石蕊试液变红色
B.小军同学认为: 实验Ⅱ喷水是多余的
C.小涛同学认为,若实验Ⅲ中的紫色小花变红,则证明假设成立
D.小芳同学对实验方案提出了质疑,她认为还需补充一个实验才能使探究活动获得成功
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。
(1)贝贝取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。结论:石蜡的密度比水 ;
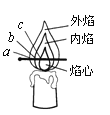
(2)芳芳点燃蜡烛,观察到火焰分为外焰、内焰、焰心三层。把一根火柴梗放在火焰中(如图)约1s后取出可以看到火柴梗的 (填“a”、“b”或“c”)处最先碳化。结论:蜡烛火焰的 温度最高;
(3)婷婷在探究蜡烛燃烧的过程中,发现罩在火焰上方的烧杯内壁被熏黑,你认为她的以下做法中不合适的是 。
A.反复实验,并观察是否有相同现象
B.查找资料,了解石蜡的主要成分,探究生成的黑色固体是什么
C.认为与本次实验目的无关,不予理睬
D.询问老师或同学,讨论生成黑色物质的原因
(4)三位同学在探究的过程中,将短玻璃导管插入焰心,发现另一端也可以点燃。
【提出问题】导管里一定有可燃性气体,气体成分可能会是什么呢?
【猜 想】贝贝认为:可能是蜡烛不完全燃烧时产生的CO
芳芳认为:可能是蜡烛受热后产生的石蜡蒸气
婷婷认为:可能以上两种情况都有
【实验方案】
换一根较长的导管,并用冷的湿毛巾包住导管,然后在导管另一端做点火实验。
【现象与结论】
如果观察到 现象,则贝贝的猜想正确;
如果观察到 现象,则芳芳的猜想正确;
如果观察到 现象,则婷婷的猜想正确。
相关试题

