【题目】化学小组同学探究“酸的化学性质”,请你参与并完成下列部分实验内容。
实验过程 | 实验现象 | 实验结论 |
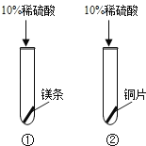
(1)
| ①号试管:固体溶解,产生气泡,放热; ②号试管: 。 | a、金属活动性: 镁 铜(填“>”或“<”) b、涉及到的化学方程式 。 |
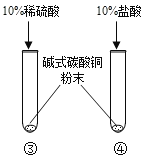
(2)
| ③号试管:绿色粉末逐渐溶解,产生气泡,溶液显蓝色。 ④号试管:绿色粉末逐渐溶解,产生气泡,溶液显绿色。 | Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑ |
【发现问题】碱式碳酸铜与稀硫酸反应形成的CuSO4溶液显蓝色,而与盐酸反应形成的CuCl2溶液显绿色。
【提出问题】同样都含有Cu2+,为什么③号试管中的CuSO4溶液显蓝色,而④号试管中的CuCl2溶液显绿色。
【猜想与假设】猜想一:若溶液中Cu2+显蓝色,则SO42+对Cu2+显色无影响,而Cl﹣对Cu2+显色有影响;
猜想二:若溶液中Cu2+显绿色,则 ;
猜想三:…
【实验验证】同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量③号试管中的溶液于另一支试管中,向其中加入 ,观察到预期实验现象,猜想一正确。
方案二:取少量④号试管中的CuCl2溶液于另一支试管中,向其中加入 ,观察到预期实验现象,猜想一正确。
【评价与反思】同学们在实验探究的过程中,体会到了溶液颜色成因复杂,相关知识还有待进一步学习。
参考答案:
【答案】【进行实验】无明显现象;>;Mg+H2SO4=MgSO4+H2↑;
【猜想与假设】SO42﹣对Cu2+显色有影响,而Cl﹣对Cu2+显色无影响;
【实验验证】适量的氯化钡溶液;适量的硝酸银溶液;(其它合理答案也可)。
【解析】
试题分析:【进行实验】因为铜排在氢的后面不能和酸反应,因此无现象;因为镁能够和硫酸反应产生氢气,说明排在氢的前面,故镁>铜;镁和硫酸反应的方程式为:Mg+H2SO4=MgSO4+H2↑;
【猜想与假设】根据猜想一,因此可以提出与之不同的猜想为:SO42﹣对Cu2+显色有影响,而Cl﹣对Cu2+显色无影响;
【实验验证】③号试管中含有的是硫酸根离子,因此可加入氯化钡等溶液使硫酸根离子产生沉淀,结果溶液由蓝色变成绿色,说明SO42+对Cu2+显色无影响,而Cl﹣对Cu2+显色有影响;
④号试管中含有的是氯离子,加入硝酸银溶液后氯离子变成沉淀,结果溶液绿色消失变成蓝色,说明SO42+对Cu2+显色无影响,而Cl﹣对Cu2+显色有影响。
-
科目: 来源: 题型:
查看答案和解析>>【题目】将少量大豆油倒入一个小铁盒中点燃,用坩埚钳把小铁盒放在冰冷的水面上,可观察到火焰立即熄灭,该实验证明,达到灭火的目的的方法之一是
A.隔绝空气 B.降低着火点
C.降温至着火点以下 D.清除可燃物
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列气体中,能供给动植物呼吸的是
A. H2 B. O2 C. N2 D. CO2
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)用100g含杂质3.2%的生铁粉(杂质不参与反应),与质量分数为10%的稀硫酸恰好完全反应制硫酸亚铁。求消耗的稀硫酸质量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人们的生产生活离不开能源。
(1)目前人们使用的燃料大多来自化石燃料,如 、石油、天然气等。
(2)开发和利用新能源是解决能源问题的重要途径。下列属于新能源的是 (填字母序号)。
A.潮汐能 B.太阳能 C.风能 D.石油
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种固体的溶解度曲线如图所示。下列说法中,不正确的是
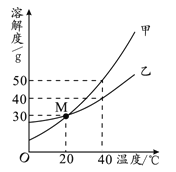
A.M点表示在20℃时,甲、乙的溶解度相同
B.40℃时,分别在100 g水中加入50 g甲、乙,充分搅拌,所得溶液中溶质的质量分数:甲大于乙
C.40℃时,分别在100 g水中加入35g 甲、乙,充分搅拌并同时降温至20℃,析出固体的质量:甲大于乙
D.20℃时,分别在50 g水中加入40 g甲、乙,充分搅拌并加热到40℃时,二者均为饱和溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】(7分)某化学兴趣小组的同学来到实验室准备做制取气体的实验。下图是实验室制取气体的常用装置:
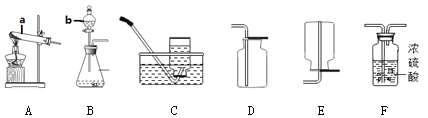
(1)请告诉小红同学,上图中标号仪器的名称a b
(2)小雨同学打算用加热高锰酸钾的方法制取氧气.该反应的化学方程式是: ,其发生装置应选 .(填字母标号,下同)
(3)小丽想用大理石和稀盐酸反应制取CO2,那她应该选择的气体收集装置是 ;
若要制得干燥的CO2 ,还应该将气体通入 装置.
相关试题