【题目】小英同学用某铁合金样品做了如下实验:称量11.4g样品,放入烧杯中,再往烧杯中加入189.2g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称得烧杯内物质总质量为200.2g。试计算(写出计算过程):
(1)反应产生氢气的质量_____。
(2)反应后所得溶液中溶质的质量分数_____。
参考答案:
【答案】0.4g 15.2%
【解析】
(1)氢气的质量:11.4g+189.2g﹣200.2g=0.4g
(2)设铁的质量为x,硫酸亚铁的质量质量为y。

![]()
解得:x=11.2g y=30.4g
反应后溶液的质量为:11.2 g+189.2g﹣0.4g=200g
反应后所得溶液溶质的质量分数为:![]() =15.2%
=15.2%
答:(1)反应产生氢气的质量为0.4g;(2)反应后所得溶液的质量分数为15.2%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图中A、B、C、D、E、F分别表示初中化学常见的六种物质,B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前提取量最大的金属,B由两种元素组成,C是大理石的主要成分。(图中用“﹣”表示两种物质之间能发生化学反应,用“→”或“
 ”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。
”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。
(1)写出F物质的化学式_____。
(2)写出C→E发生反应的化学方程式_____。
(3)B与D发生化学反应的基本类型是_____。
(4)写出少量A的粉末与过量的B发生反应的实验现象_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列是实验室制取气体的常用装置,请回答相关问题:
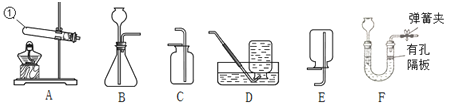
(1)写出仪器①的名称:_____。
(2)实验室用高锰酸钾制备并收集较纯净氧气应选用的装置是_____(填序号)。若用D装置收集氧气时,待集气瓶里的水排完后,接着_____,然后小心地把集气瓶移出水槽,正放在桌面上。
(3)装置B作为气体发生装置对反应物状态和反应条件的要求是_____;用装置C来收集CO2,其验满的方法是_____。 若用装置F制备CO2,其优点是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
(查阅资料)(1)、固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
(2)、氯化钙溶液和酒精溶液均呈中性。
(提出问题)固体酒精中的氢氧化钠是否变质?
(实验探究)
(1)、取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的_____,由此说明氢氧化钠已变质。
(2)、为进一步确定氢氧化钠的变质程度,分组进行探究。
甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案
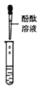
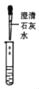
实验现象
溶液变红
产生_____
实验结论
清液中有氢氧化钠
清液中有碳酸钠
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_____。
他们另取烧杯中上层清液,加足量氯化钙溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)(1)、乙组实验中加足量氯化钙溶液的目的是_____。
(2)、乙组实验中能否用澄清石灰水代替氯化钙溶液_____(填“能”或“不能”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】量取8mL水稀释浓硫酸的下列操作正确的是( )
A. 向10mL量筒中加水接近8mL

B. 再用滴管滴水至8mL

C. 把水加入浓硫酸中
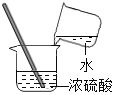
D. 搅拌
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关叙述、对应的方程式,所属基本反应类型都正确的是( )
A. 工业炼铁:3C+2Fe2O3
 4Fe+3CO2↑ 置换反应
4Fe+3CO2↑ 置换反应B. 实验室用稀硝酸与锌粒反应制取氢气:Zn+2HNO3=Zn(NO3)2+H2↑ 置换反应
C. 洗去试管上附着的铜:Cu+H2SO4=CuSO4+H2↑ 置换反应
D. 铝制品抗腐蚀:4Al+3O2
 2Al2O3 化合反应
2Al2O3 化合反应 -
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列有关叙述正确的是( )
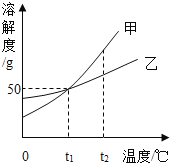
A. t1℃时,甲物质的溶解度是50
B. 温度低于t1℃时,甲物质溶解度大于乙物质
C. t2℃时,将甲、乙两物质的饱和溶液降温至t1℃,甲溶液析出晶体的质量大于乙
D. 甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯甲
相关试题

