【题目】根据下列方框图回答下列问题:
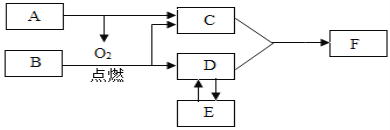
已知:A、B、C、D、E都是初中化学常见的物质。A和C在常温下均为无色液体,B是由两种元素组成的清洁能源;D与E含有相同的两种元素,且D参与植物的光合作用;F含有A﹣E的所有元素。
(1)请推断物质的化学式:B______、F_______。
(2)写出物质A转化为C的化学方程式___________。
(3)写出D转化为E的化学方程式_________,基本反应类型为_________反应。
参考答案:
【答案】CH4 H2CO3 2H2O2![]() 2H2O+O2↑ CO2+C
2H2O+O2↑ CO2+C![]() 2CO 化合
2CO 化合
【解析】
A、B、C、D、E都是初中化学常见的物质,A和C在常温下均为无色液体,A会生成氧气和C,所以A是过氧化氢溶液,C是水,B是由两种元素组成的清洁能源,所以B是甲烷,D与E含有相同的两种元素,且E是有毒气体,所以E是一氧化碳,一氧化碳和D可以互相转化,所以D是二氧化碳,甲烷和氧气在点燃的条件下生成水和二氧化碳,F含有A-E的所有元素,水和二氧化碳反应生成碳酸,所以F是碳酸,经过验证,推导正确。
由分析可知(1)所以B是CH4,F是H2CO3;
(2)物质A转化为C的反应是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)D转化为E的反应是二氧化碳和碳在高温的条件下生成一氧化碳,化学方程式为:CO2+C![]() 2CO,该反应属于化合反应。
2CO,该反应属于化合反应。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“见著知微”是化学学习者应该具备的基本素养,也是学习化学的重要思想方法。
资料一:

资料二:氟及其化合物常运用于原子弹制造、航天工业等领域。氟气(F2)化学性质极其活泼,水都能在氟气中燃烧,且燃烧产物是氧气。结合以上信息,回答下列问题:
(1)氮原子核外有__________个电子层,图B中x=________。
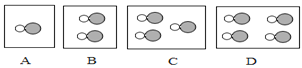
(2)如图是水与氟气反应的微观示意图。图中方框内应填图中的__________选项,选择此选项的理由是________。

(3)作为航天大国,我国自主研发的运载火箭型号众多。某型火箭曾采用N2H4和H2O2作为火箭推进剂,N2H4和H2O2在点燃条件下生成一种常温下为液态的氧化物和一种单质,反应的化学方程式为_____,该反应是_______ (填“放热”或“吸热”)反应。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验是学习化学的一种重要途径,实验室用下图所示装置制取并收集气体。

请回答下列各题:
(l)仪器①的名称是_________,②的名称是__________。
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是_______;若用排水法收集氧气时不能刚有气泡就开始收集,原因是_______。
(3)既能收集氧气也能收集二氧化碳气体的装置是____(填序号),检验瓶中气体是否为二氧化碳可用_____ (填药品名称)。
(4)乙炔(C2H2)气体可用电石(CaC2块状固体)和水反应来制取,化学方程式为CaC2+2H2O
 Ca(OH)2+C2H2↑,实验室制取乙炔(C2H2)气体的发生装置应选用___(填序号)。
Ca(OH)2+C2H2↑,实验室制取乙炔(C2H2)气体的发生装置应选用___(填序号)。 -
科目: 来源: 题型:
查看答案和解析>>【题目】能源、环境与人类的生活和社会发展密切相关,合理利用能源和保护环境是我们关注的问题。请根据所学化学知识回答下列问题:
(1)目前,人类使用的化石燃料主要包括______、石油、天然气三种。
(2)可燃冰,学名天然气水化合物,其外观像冰,在地球上的储量大约是已探明其他化石燃料总量的2倍。写出可燃冰完全燃烧的化学方程式_________。
(3)常在普通汽油中加入适量的乙醇,形成乙醇汽油作为燃料。对乙醇汽油作汽车燃料的优点是___。
(4)化石燃料的燃烧会引发许多环境问题。如燃烧产生的二氧化碳气体在空气中含量增多会导致_____。请你从减少二氧化碳产生的角度提一条减缓该环境问题的措施____。
-
科目: 来源: 题型:
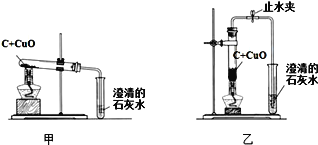
查看答案和解析>>【题目】木炭作为还原剂用于金属冶炼已有几千年历史。化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,他们决定对这个实验进行探究和改进。
(1)木炭与氧化铜反应的化学方程式是________。
(2)小波建议用超细炭粉与氧化铜粉末混合进行实验,你认为这样建议的原理是_______。
(3)小周建议用图乙装置替代图甲装置。与图甲相比较,图乙装置中将试管直立放置、将反应混合物夯实于试管底部,并通过调节酒精灯可使外焰完全包围试管的下部,这样设计的原因是________。
(4)检查了乙装置的气密性后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,_______(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
(5)待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是___。待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室新进一批大理石,某化学小组为测定碳酸钙的含量,称量17.5g该大理石样品,加入50.0g(足量)稀盐酸放入烧杯,完全反应后,称得烧杯内剩余物质质量为60.9g。样品中杂质不溶于水也不与稀盐酸反应,生成的气体完全逸出,则:
(1)17.5g该样品最多可制得二氧化碳的质量为 _______。
(2)计算该样品中碳酸钙的质量分数_________。(计算结果精确到0.1%)
-
科目: 来源: 题型:
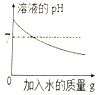
查看答案和解析>>【题目】下列图象能正确反映对应变化关系的是( )
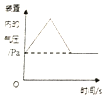
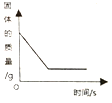
A.足量红磷在密闭容器中燃烧
B.常温下,稀释KOH 溶液
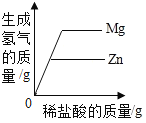
C.向等质量的Mg和Zn中分别加入等质量等浓度的稀盐酸
D.将铁钉加入一定量的硫酸铜溶液中
A. A B. B C. C D. D
相关试题

