【题目】KCl和KNO3的溶解度表及溶解度曲线如下图所示,下列说法不正确的是 ( )
温度/℃ | 20 | 30 | 40 | 50 | |
溶解度S/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
A. 甲表示KCl溶解度曲线 
B. 温度t1应在20℃~30℃之间
C. 40℃时,5gKCl加入10g水中,可得到33.3%的溶液
D. 50℃时,30g KNO3加入50g水,充分溶解,再降温到30℃,有晶体析出
参考答案:
【答案】AC
【解析】A、硝酸钾的溶解度受温度影响变化大,故甲表示KNO3溶解度曲线,故错误;B、t1℃时二者的溶解度相等,根据表格看出,该温度应该介于20℃~30℃之间,故正确;C、40℃时氯化钾的溶解度是40.0g,即100g水中最多溶解40.0g的氯化钾,所以5gKCl加入10g水中最多溶解4g,溶质的质量分数是: ![]() ×100%≈28.6%,故错误;D、50℃时硝酸钾的溶解度是85.5g,所以30g KNO3加入50g水,充分溶解不饱和,再降温到30℃,其溶解度变为45.8g,50g水中最多溶解22.9g,所以有晶体析出,故正确;故选AC。
×100%≈28.6%,故错误;D、50℃时硝酸钾的溶解度是85.5g,所以30g KNO3加入50g水,充分溶解不饱和,再降温到30℃,其溶解度变为45.8g,50g水中最多溶解22.9g,所以有晶体析出,故正确;故选AC。
-
科目: 来源: 题型:
查看答案和解析>>【题目】环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
(1)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减缓温室效应,我们可以采取的措施有(只填2种):________________;_____________。
(2)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。已知温度越高、压强越小,气体在水中溶解得越少。
A、 二氧化碳气体转变为液体时将会__________能量(填“释放”或“消耗”);
B、二氧化碳使海水酸度增加的原理的反应表达式为_________ ;
C、二氧化碳在深海中比在通常状况下的水中的溶解得(填“多”或“少”)_______,原因是_____________。
(3)二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加。
A、二氧化碳和水通过光合作用转变为葡萄糖和氧气的反应表达式为:_______________。
B、我国科学家陈乾旺等最新研究成果表明,在一定条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,请从人类生存的角度分析,金刚石与水相比谁更宝贵______,理由是_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲和乙可以制备化工原料丙,微观过程如下图。下列说法错误的是( )

A. 丁的化学式为O2
B. 丙中C、H的质量比为12:1
C. 该反应体现无机物可转化为有机物
D. 若改变反应条件,甲和乙反应可生成一种重要的糖类物质
-
科目: 来源: 题型:
查看答案和解析>>【题目】在NaOH和Na2CO3的混合物9.3g中加入一定量的10.0%的稀盐酸,恰好完全反应, 将生成的气体全部通入足量的澄清石灰水中,产生5.0g沉淀。下列说法正确的是( )
A. 题中的一定量是7.3g
B. 反应共产生11.7gNaCl
C. 如用10%的稀盐酸将5.0g沉淀溶解,则所用稀盐酸的量与题中的一定量相等
D. Na2CO3消耗的稀盐酸比NaOH消耗的稀盐酸多
-
科目: 来源: 题型:
查看答案和解析>>【题目】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是( )
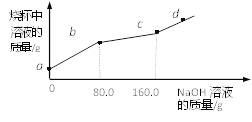
A. ab段反应产生蓝色沉淀
B. bc段溶液增加70.2g
C. c点对应的溶质质量分数为4.9%
D. d点溶液显碱性
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。流程简图如下(已知:母液中有一种铵态氮肥) ,下列有关说法不正确的是 ( )
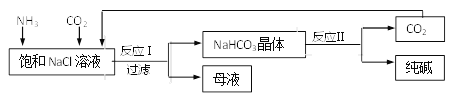
A. 反应中先通入氨气的目的是促进二氧化碳的吸收,提高产率
B. “母液”中一定只含有两种溶质
C. 反应II得到的CO2可以循环使用
D. 反应I的方程式为NaCl+NH3+CO2=NaHCO3↓+NH4Cl
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图为半透膜淡化海水分离技术示意图。对海水加压,水分子可以通过半透膜形成淡水,而海水中的其它物质不能通过渗透膜。
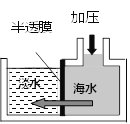
(1)采用此分离技术所得到的淡水的硬度_______(选填“高”或“低”)。
(2)对所得淡水进行“矿化”处理来可提高饮用水品质。用CO2酸化的淡水浸泡石灰石使其部分“转化”为可溶的碳酸氢钙Ca(HCO3)2,达到“矿化”的目的。“转化”过程的化学反应方程式为____________。
相关试题

