【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。
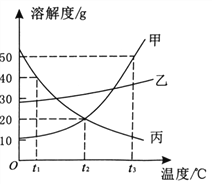
⑴t2℃时甲的溶解度为________________;t1℃时将30g丙加入到50g水中溶解形成溶液的质量为____________。
⑵丙的饱和溶液中含有少量的甲,由该液体提纯固体丙,结晶的方法是________(填序号,下同)。
A.蒸发溶剂 B.降低温度 C.升高温度
⑶下列说法正确的是_________。
A.t3℃时,等质量的甲、乙、丙恰好形成的饱和溶液中含溶剂最多的是丙
B. t3℃时,等质量的甲、乙、丙的饱和溶液降温至t2℃,所得溶液中溶质质量分数是乙>甲>丙
C.t2℃时,向乙的饱和溶液中加入固体乙,溶质的质量分数不变
D.将三种物质的溶液从t3℃降温至t1℃,析出晶体最多的是甲
参考答案:
【答案】 20g 70g C ABC
【解析】(1)通过分析溶解度曲线可知,t2℃时,甲物质的溶解度为20g;t1℃时,丙物质的溶解度为40g,将30g丙加入到50g水中溶解形成溶液的质量为20g+50g=70g;(2)通过分析溶解度曲线可知,丙的溶解度随温度的升高而减小,丙的饱和溶液中含有少量的甲,由该液体提纯固体丙,结晶的方法是升高温度;(3)A、通过分析溶解度曲线可知,t3℃时,甲、乙、丙的溶解度的关系为:甲>乙>丙;所以等质量的甲、乙、丙恰好形成的饱和溶液中含溶剂最多的是丙,故正确;B、通过分析溶解度曲线可知,t3℃时,等质量的甲、乙、丙的饱和溶液降温至t2℃,所得溶液中溶质质量分数是乙>甲>丙,故正确;C、t2℃时,向乙的饱和溶液中加入固体乙,乙不再溶解,所以溶质的质量分数不变,故正确;D、将三种物质的溶液从t3℃降温至t1℃,因为不知道溶液的质量,析出晶体的多少无法比较,故错误。
-
科目: 来源: 题型:
查看答案和解析>>【题目】正确使用化学用语是重要的化学学科素养,下列说法正确的是( )
A. H2O、H2O2、H2SO4 中均含有氢分子
B. 右图表示的粒子都是阳离子
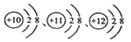
C. KCl、KClO、KClO3中氯元素的化合价相同
D. CO、CO2、H2CO3都是含碳元素的化合物
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学用语填空
(1)2个氮原子__________;
(2)8个硫原子构成的分子_______;
(3)硫酸铜的构成微粒有Cu2+和_____________;
(4)氨气中氮元素的化合价_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
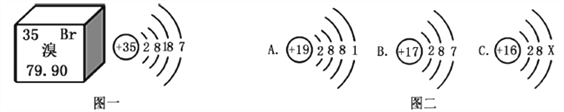
①溴的相对原子质量是_______。
②溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
③溴元素与图二中A元素形成化合物的化学式为:_______。
(2)下面是某化学反应前后的微观模拟图(反应条件省略):
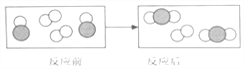
该化学反应中,参加反应的
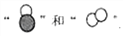 与反应后生成
与反应后生成 的各粒子间的个数比为_________。
的各粒子间的个数比为_________。 -
科目: 来源: 题型:
查看答案和解析>>【题目】下图是实验室制取气体的装置。
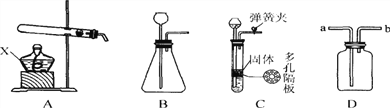
(1)写出仪器X的名称:______________
(2)写出用A装置制取O2的化学方程式____________________。若用D装置收集O2,气体应从 ________(填a或b)通入。
(3)B和C装置均可制取CO2,实验室欲制取CO2,且多次进行有关性质的验证实验,应选择C装置,选择该装置的理由是_______________________。
(4)用足量的锌粒与稀硫酸按C装置制取一定量较纯的氢气。当发现液面不能与锌粒接触,此时又无酸液可加,若从长颈漏斗中加入适量下列试剂,不影响生成氢气的量。你认为不能加入的试剂是_____________(填编号)。
A.稀盐酸 B.硫酸钠溶液 C.碳酸钠溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图。
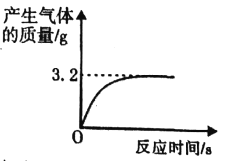
(1)完全反应后,经过滤、烘干,得到固体的质量为_______(不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是_______。
A.二氧化锰越来越少
B.过氧化氢溶液的溶质质盘分数越来越小
D.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数。(规范写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、 B、 C、 D、 E 为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质, “-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答下列问题。
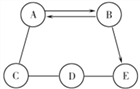
(1)若 A可作绿色植物光合作用的原料,B、C、E 都是含钙元素的化合物,B、E同属盐类物质。则 B 的化学式为_____________,物质 D 的类别为___________。(填酸、碱、 盐或氧化物)。
(2)若B常温下呈液态,C是红棕色固体,且B、C均属氧化物。
①A﹣C反应的基本类型是_______。
②B→E 反应的化学方程式是__________________________。
相关试题

