【题目】向含CuCl2和HCl的100 g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2。则下列说法正确的是 ( )
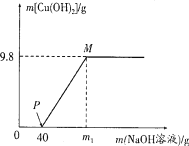
A. 整个反应过程中,溶液中氯离子个数不变
B. PM段的溶液中加入铁粉,会产生气泡
C. M点溶液中氯化钠的质量分数为8.3%
D. 沉淀完全时,m1的数值为80
参考答案:
【答案】AC
【解析】化学反应过程只是原子重新组合的过程,反应前后原子的种类、个数不变。向含CuCl2和HCl的100 g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,氢氧化钠和氯化铜反应生成氢氧化铜和氯化钠,盐酸和氢氧化钠反应生成氯化钠和水。A.因为只生成氢氧化铜沉淀,故A选项整个反应过程中,氯离子个数都存在于溶液中,所以溶液中氯离子个数不变;B.向混合物中加入氢氧化钠时,盐酸先和氢氧化钠反应,所以P点溶液中的溶质有两种氯化钠和氯化铜,PM段的溶液中加入铁粉,发生的反应是铁和氯化铜生成铜和氯化亚铁,所以不会产生气泡;C. 设氢氧化钠和盐酸反应生成氯化钠的质量为x
HCl + NaOH==H2O+NaCl
40 58.5
40g×10% x
40/ 40g×10%=58.5/x x=5.85g
设氢氧化钠和氯化铜反应生成氯化钠的质量为y
CuCl2+2NaOH==Cu(OH)2↓+2NaCl及有关数据可知是正确的叙述;
80 98 117
z 9.8g y
98/9.8g=117/y y=11.7g
98/9.8g=80/z z=8g 和氯化铜反应的氢氧化钠溶液的质量为:8g÷10%=80g
M点氯化钠的质量为11.7g+5.85g=17.55g
M点溶液的质量为40g+80g+100g-9.8g=210.2g
M点溶液中氯化钠的质量分数为17.55g÷210.2g ×100%≈8.3%,
D. 沉淀完全时,m1的数值为80g+40g=120g
选AC
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一瓶纯碱(Na2CO3)固体中混有少量烧碱(NaOH),现在需要测出这瓶药品中烧碱的含量,便取固体药品12g置于含水100g烧杯中,搅拌至完全溶解,并滴加几滴酚酞试液,溶液呈红色;再滴加稀盐酸,当用去稀盐酸100g时,溶液恰好变成无色。 反应前后质量关系如表:
反应前
反应后
固体样品
水
稀盐酸
剩余液体
12g
100g
100g
207.6g
请回答:
(1)整个反应生成气体_______g
(2)原固体样品中含纯碱(Na2CO3)_____________g
(3)计算出使用的稀盐酸的溶质质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中)。当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了。根据以上现象请你分析下列说法不正确的是( )
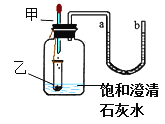
A. 甲、乙可能分别是稀盐酸和大理石
B. 甲、乙可能分别是水和生石灰
C. 甲、乙可能分别是稀盐酸和镁条
D. 石灰水变浑浊,一定是发生了化学变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:
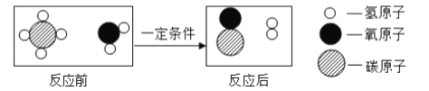
根据以上微观示意图得出的结论中,正确的是( )
A. 反应前后各元素的化合价均不变
B. 水煤气的成分是一氧化碳和氢气
C. 该反应中含氢元素的化合物有3种
D. 该反应的化学方程式中,两种生成物的计量数之比为1:1
-
科目: 来源: 题型:
查看答案和解析>>【题目】KCl和KNO3的溶解度表及溶解度曲线如下图所示,下列说法不正确的是 ( )

A. 甲表示KCl溶解度曲线
B. 两物质溶解度相等的温度t1在20℃~30℃
C. 40℃时,5gKCl加入10g水中,可得到33.3%的溶液
D. 50℃时,30g KNO3加入50g水,充分溶解,再降温到30℃,有晶体析出
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合图示实验装置,回答下列问题:

(1)图中a、b仪器的名称:a__________,b__________.
(2)某同学在实验室用C装置制取二氧化碳,反应的化学方程式为____________,C装置与B装置相比较,优点为__________________
(3)实验室用B装置制取氧气时,锥形瓶中应先加入试剂为__________.如要获得干燥的气体,除发生装置外,还应选用盛放__________(填写试剂名称)的D装置.如用E装置收集CO2,则气体应从______端通入(填“c”或“d”).
(4)实验室用熟石灰与硫酸铵共热制取氨气,应选_________发生装置,反应的化学方程式为__________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学用语是学习化学的重要工具.
(1)写出下列对应的化学符号:
① 铝离子 ___________ ;② 硝酸分子 __________;③ 5个硅原子____________
④ 氦气 _________ ;⑤ 人体中最多的物质__________ ;⑥ 最简单的有机物______
(2)用下列字母序号填空:
a.硫酸铜 b.氯化钠 c.熟石灰 d.石墨
①_____________用作调味品和防腐剂;②_____________用作改良酸性土壤;
③_____________用配制波尔多液; ④_____________用作电极材料;
(3)写出下列反应的化学方程式:
① 湿法冶金:__________________________;
② 铝的自我保护__________________________;
③ 光合作用:__________________________;
④ 氢氧化钠在空气中变质:__________________________;该反应_____________复分解反应(填“属于”或“不属于”)
相关试题

