【题目】下面五环图种的每个环代表初中化学中常见的一种物质,它们分别属于单质、氧化物、酸、碱、盐中的一种。相邻两环相绕表示两种物质之间在常温下能相互反应。

(1)请写出五环图中A、B、C、D、E五种物质的化学式:_____,_____,_____,_____,_____。
(2)写出C和D反应的化学方程式:_____;
参考答案:
【答案】Zn H2SO4 Na2CO3 Ca(OH)2 CO2 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【解析】
A可以是活泼金属,如Zn,B可以是稀H2SO4,Zn+H2SO4=ZnSO4+H2↑,稀H2SO4属于酸,酸能与盐、碱、金属氧化物反应,但金属氧化物不能与盐、碱反应,所以C不能是金属氧化物,如果C是碱,则D是盐,盐不能与氧化物反应,所以C只能是盐,D是碱,E是非金属氧化物。C可以是Na2CO3,Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,D是Ca(OH)2,Na2CO3+Ca(OH)2 =CaCO3↓+ 2NaOH,E是CO2,CO2+Ca(OH)2=CaCO3↓+H2O。
(1)A、B、C、D、E五种物质的化学式分别是Zn、H2SO4、Na2CO3、Ca(OH)2、CO2。
(2)C和D反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
-
科目: 来源: 题型:
查看答案和解析>>【题目】向盛有稀硫酸和硫酸铁的混合液的烧杯中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列分析正确的是

A. 向oa段(不含a点)溶液中滴入紫色石蕊试液变红
B. 到达b点时,烧杯内的溶液中含有两种溶质
C. 到达b点时,所消耗氢氧化钠溶液中溶质的质量是12g
D. 整个变化过程烧杯内的溶液中硫酸根离子数目没有改变
-
科目: 来源: 题型:
查看答案和解析>>【题目】青少年正处在生长发育期应注意营养均衡,胼食合理。
(1)有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入_____(选填序号)不足而引起的。
A 油脂 B 维生素 C 蛋白质 D 糖类
(2)“XX糕点”主要营养成分如表所示。请根据该表回答:

①正常情况下,人每日摄入的油脂不超过60g。由此计算,每日食用该糕点最多不应超过____g
②糖类物质是人体所需能量的主要来源;它在人体内分解、氧化释放出能量的过程,是将_____能转化为热能。
③人体缺_____能导致青少年发育不良或佝偻病,该糕点中的______可以补充这种元素。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学实验是进行科学探究的重要手段。请你参与探究并填空:
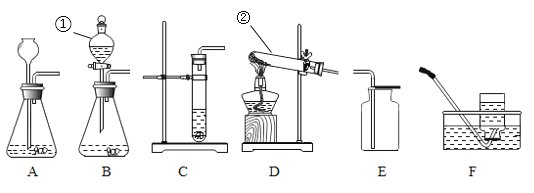
(1)写出图中标号仪器的名称:①______;②______;
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时,发生反应的化学方程式为_____;
(3)实验室用过氧化氢溶液和二氧化锰制取氧气、用石灰石和稀盐酸制取二氧化碳,发生装置都可以选用上图A、B、C所示的实验装置,请分析选择的理由是_____。请分析在实验室制取以上两种气体,发生装置最好选用B所示装置的理由:______。
(4)可用图F所示的方法收集氧气,主要是因为氧气_____。在收集气体前,图F中集气瓶内装满水的目的是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如图实验。已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。
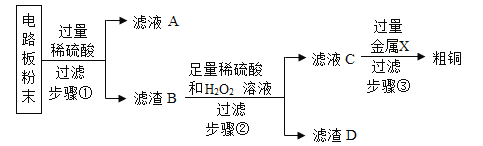
(1)将电路板粉碎成粉末的目的是_____。
(2)写出一个步骤①中发生反应的化学方程式_____。
(3)滤液A中的阳离子有_____。
(4)步骤②的目的是_____。
(5)要除去粗铜中的杂质,不能选用_____。(选填字母序号)
A 氯化铜溶液 B 稀盐酸 C 蒸馏水
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表为氯化钠、碳酸钠在水中的溶解度。我国西北地区有很多咸水湖,其中最大的是柴达木盆地的察尔汗盐池。某盐湖附近的农民通过“冬天捞碱.夏天晒盐”获得大量湖盐。这里的“碱”指纯碱(主要成分是碳酸钠) ,盐指氯化钠。
温度/℃
0
10
20
30
40
溶解度
氯化钠
35.7
35.8
35.9
36.1
37.1
碳酸钠
7.0
12.5
21.5
39.7
49.0
(1)请据图表简要解释“冬天捞碱,夏天晒盐”其中的道理____。
(2)小勤同学取该湖盐样品进行探究。
(提出问题)该湖盐样品的成分是什么?
(猜想与假设)猜想一:只有Na2CO3:猜想二:只有NaCl;猜想三:Na2CO3和NaCl。
(实验探究)
实验操作
实验现象
实验结论
取少量样品于试管中,向其中加入足量的____溶液;过滤,得沉淀和滤液,向沉淀中加入足量稀硝酸
产生白色沉淀
部分白色沉淀消失
猜想三成立
(拓展延伸)为进一步确定该湖盐样品中Na2CO3的质量分数,小勤同学再取该湖盐样品10.00g做了如图所示的补充实验(假定每步均完全反应或吸收)。
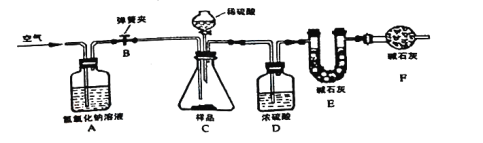
①反应结束之后通入足量空气的目的是_____。
②装置A中氢氧化钠溶液的作用是_____(用化学方程式表示)。
③实验结束后测得装置E增重0.44g,请根据上图所示的实验过程和提供的数据计算该湖盐样品中碳酸钠的质量分数是多少_____?(写出计算步骤,计算结果精确到0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组在实验室里探究某些酸、碱、盐之间是否发生复分解反应。请你参与探究并填空:
(查阅资料)①硫酸铜和氯化铜的溶液都有毒。铜离子可以使蛋白质变性,可以杀死细菌和病毒,可以破坏人体细胞。②硫酸钠溶液呈中性,无毒。
(实验与探究)
内容
现象
实验解析
结论
实验一
取少量稀盐酸于小试管中,滴入数滴碳酸钠溶液,振荡
_____
化学方程式:
Na2CO3+2HCl==2NaCl+H2O+CO2↑
生成物中有____或有____或有____生成时,复分解反应可以发生。
实验二
取少量氢氧化钠溶液于小试管中,滴入几滴酚酞试液振荡,液体呈现红色;再滴入足量的稀硫酸
_____
实验三
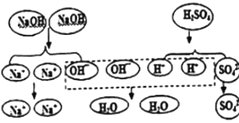
取少量氯化铜溶液于小试管中,滴入几滴氢氧化钠溶液试液,振荡
_____
该反应的微观实质是:______;
(废液处理)实验结束时,老师指出,废液定要进行无害化处理,尽量实现绿色排放(不考虑酚酞试液)。同学们把三个实验的试管内所有物质都倒入一个洁净的烧杯中得到蓝色澄清液体。根据上述现象,同学们向废液中逐滴滴加_____溶液,直至观察到_____。说明废液达到了绿色排放的要求。
相关试题

