【题目】被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的双氧水(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体。在化学实验开放日,实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体,请填写有关内容:_________ ___________
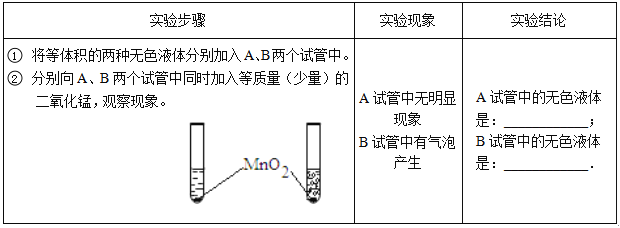
⑴写出B试管内产生气体的化学符号表达式:__________________________,该反应是________(选填“吸热”或“放热”)反应
⑵如何检验B试管中产生的气体(写出操作步骤、实验现象和实验结论)______________。
参考答案:
【答案】 水 双氧水 2H2O2![]() 2H2O+O2↑ 放热 将带火星的小木条伸入试管,如果木条复燃,证明是氧气
2H2O+O2↑ 放热 将带火星的小木条伸入试管,如果木条复燃,证明是氧气
【解析】实验在常温下进行,常温下过氧化氢在二氧化锰催化下可以迅速分解出氧气,而水不能发生分解;故加入二氧化锰后,有气泡产生的液体为过氧化氢溶液,无现象的为水;(1)过氧化氢分解时,加入的二氧化锰是催化剂,2H2O2![]() 2H2O+O2↑,该反应放出热量;(2)实验室检验氧气使用带火星的木条,能使之复燃气体则为氧气。
2H2O+O2↑,该反应放出热量;(2)实验室检验氧气使用带火星的木条,能使之复燃气体则为氧气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室里,在一个具有刻度和可以滑动的活塞的玻璃管中放入白磷(过量,白磷燃烧所需的最低温度为40 ℃,燃烧现象及产物均与红磷相同 ),将玻璃管固定好,放在盛有80 ℃热水的烧杯上,实验装置如图1所示,试回答下列问题。
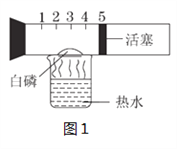

(1)整个实验过程中,可以观察到的现象有:
①玻璃管内______________________;
②活塞________________________________________________;
③活塞最后约停在刻度_______处。
白磷在反应过程中要过量的原因是_________________________________。
(2)图2为书本上测定空气中氧气含量的实验装置,图1和图2相比,你认为哪种装置更好?理由是什么?___________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有下列初中化学常用的制取气体的部分装置。据此请完成以下各题:
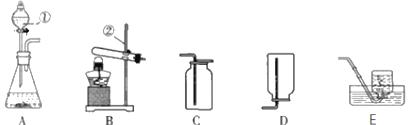
(1)写出上图①、②两种仪器的名称:①_______、②_______。
(2)以高锰酸钾为原料制取并收集纯净的氧气,应选用_______(填字母)装置,反应的符号表达式是_______________________。若采用排水集气法收集氧气时,发现水槽中的水变红了,可能的原因是_______________________________;
(3)用高锰酸钾制取氧气,下列有关实验操作的先后顺序及其原因的阐述中,正确的有__________。
A.将导气管插入橡皮塞时:先用水湿润导气管,后插入橡皮塞;起润滑作用
B.检查装置气密性时:先装药品,后检查装置气密性;符合简捷原则
C.加热时:先预热,后将火焰对准药品所在部位加热;以免试管受热不均而破裂
D.加热时,看到水槽中有气泡放出,立即开始收集氧气,否则会导致氧气浪费。
(4)某同学在做氧气实验时,发现试管炸裂,造成此结果的原因不可能是 (______)
A.加热前未将试管外壁擦干 B.加热前试管未均匀受热
C.加热时将试管口略向下倾斜 D.反应停止时,先熄灭酒精灯
(5)用过氧化氢溶液和二氧化锰混合制取氧气应选用的发生装置是_______(填序号),发生反应的化学符号表达式为___________________。
(6)某老师带领学生进行上述实验时,发现一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃;于是,老师让该同学重新做实验:先往集气瓶中装入半瓶水,再用排水法收集1/2集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃。
①用下列方案收集“1/2集气瓶的氧气”,其中最合理的是_______(填字母)。
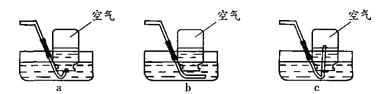
②用排水法收集气体时,如何判断集气瓶中气体已收集满?
答:________________________________________ 。
③空气中氧气的体积分数约为21%。本实验中,该同学收集的集气瓶内的氧气约占总体积的_______%,所以用“使带火星的木条复燃”来检验集气瓶中充满氧气的方法并不能保证收集到的氧气很纯净。
-
科目: 来源: 题型:
查看答案和解析>>【题目】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】右下图是他们进行实验的装置图,气体发生装置中A仪器的名称是_____________,此实验中B处宜采用的气体收集方法是_______ _____。
【实验记录】
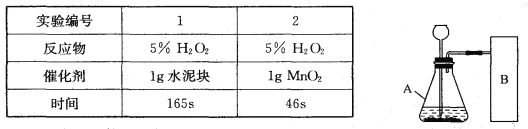
【结论】该探究过程得出的结论是_________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____ _____是否改变。
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤
现 象
结 论
取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰。
缓慢有少量气泡冒出
另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰。
迅速有大量气泡冒出
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤
现 象
结 论
温度越高,过氧化氢分解的速率越大
-
科目: 来源: 题型:
查看答案和解析>>【题目】正确使用化学用语是重要的化学学科素养,下列说法正确的是( )
A. H2O、H2O2、H2SO4 中均含有氢分子
B. 右图表示的粒子都是阳离子
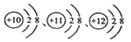
C. KCl、KClO、KClO3中氯元素的化合价相同
D. CO、CO2、H2CO3都是含碳元素的化合物
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学用语填空
(1)2个氮原子__________;
(2)8个硫原子构成的分子_______;
(3)硫酸铜的构成微粒有Cu2+和_____________;
(4)氨气中氮元素的化合价_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
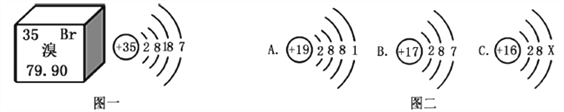
①溴的相对原子质量是_______。
②溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
③溴元素与图二中A元素形成化合物的化学式为:_______。
(2)下面是某化学反应前后的微观模拟图(反应条件省略):
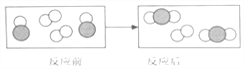
该化学反应中,参加反应的
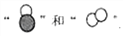 与反应后生成
与反应后生成 的各粒子间的个数比为_________。
的各粒子间的个数比为_________。
相关试题

