【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 42 | 109 | 129 | 174 | 314 | 347 | |
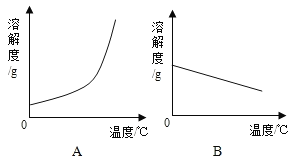
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示Ca(OH)2溶解度曲线的是_______(填“A”或“B”)。
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,有下列措施:①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度。其中均可行的一组是______(填序号)
A.①②④ B.②③④ C.①③⑤ D.①②⑤
(3)20℃时,200g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH晶体的质量为________g。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量的CaO固体后,恢复到20℃,得到的溶液(乙溶液),已知:CaO + H2O = Ca(OH)2 。 则甲乙溶液中溶质的质量分数的关系为ω(乙)_____ω(甲)(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是________。
参考答案:
【答案】 略 略 略 略 略
【解析】(1)由表可知,氢氧化钠的溶解度随温度的升高而升高,氢氧化钙的溶解度随温度的升高而降低,故Ca(OH)2溶解度曲线的是A;
(2)氢氧化钙的溶解度随温度的升高而降低,故可以加入溶质,降低温度是不饱和的氢氧化钙溶液变为饱和溶液,①②⑤正确,故选D;
(3)20℃时,氢氧化钠的溶解度为109g,故10g水中能溶解氢氧化钠的质量是10.9g;
(4)向饱和的氢氧化钙溶液中加入氧化钙后,氧化钙可以与水反应生成氢氧化钙,反应耗掉了水分,生成了氢氧化钙,故有氢氧化钙析出,由于温度没变,故溶质的质量分数不变;
(5)氢氧化钠的溶解度随温度的升高而升高,氢氧化钙的溶解度随温度的升高而降低,故可以采用降温结晶的方法提取氢氧化钠;
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验。
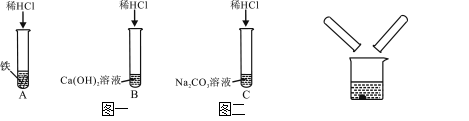
(1)A试管中的反应现象是 。
(2)C试管中反应的化学方程式是 。
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、 HCl
你的猜想:有 。
【交流讨论】
你认为 同学的猜想一定不正确,理由是 。
【设计实验】请设计实验证明你的猜想正确。
实验步骤
实验现象
实验结论
取少量滤液于试管中,向其中滴加 。
_________________。
我的猜想成立
【反思与总结】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类对材料的发现和使用经历了从石器、青铜器、铁器到铝的大规模使用等漫长的征程。请回答:
(1)我国是最早采用湿法冶铜的国家。文献记载“胆铜法”:用铁与“胆水”(含CuSO4)反应获得铜。铁与硫酸铜溶液反应的化学方程式为________;
(2)下列金属矿物中,可以用来炼铁的是______(填正确选项前的字母);
A. 赤铜矿(Cu2O) B.赤铁矿(Fe2O3) C.软锰矿(MnO2)
(3)生活中人们喜欢用铝制品的一个重要因素是它难生锈,铝制品难生锈原因是:______________。
(4)为比较铜和铁的金属活动性,某同学设计实验方案:将大小相同的铜块和铁块分别放入相同浓度的稀盐酸中,比较反应的剧烈程度。你认为该方案__________________(填“合理”或“不合理”),理由是_____________。
(5)我国的高铁技术世界领先.高铁钢轨采用铝和氧化铁在高温下发生置换反应实现无缝焊接,该反应的化学方程式为_____________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】水钢采用烟气脱硫工艺,不仅能消除二氧化硫,防止形成酸雨,还能将其转化为硫酸钙等产品,实现“变废为宝”。反应的化学方程式为:2CaCO3+O2+2SO2
 2CaSO4+2CO2,现用2.5t含碳酸钙80%的石灰石吸收烟气中的二氧化硫。求:
2CaSO4+2CO2,现用2.5t含碳酸钙80%的石灰石吸收烟气中的二氧化硫。求:(l)所用石灰石中含碳酸钙的质量。
(2)理论上可吸收二氧化硫的质量(要求有计算步骤)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】向100 g9.8%的稀硫酸中逐滴加入8%的氢氧化钠溶液至200g,测得硫酸的质量分数与加入的氢氧化钠溶液质量的关系如下图所示,计算回答:

(1)据上左图分析:加入氢氧化钠溶液______g时与100g稀硫酸恰好完全反应。
(2)计算坐标中a点相应的值是_______________?(写出计算过程,保留小数点后一位,下同)
(3)计算往稀硫酸中加入氢氧化钠溶液至200g时所得溶液中硫酸钠的质量分数___________?
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是硝酸钾的溶解度曲线,回答下列问题:
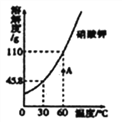
(1)硝酸钾的溶解度随温度升高而______________ ;
(2)当温度为__________℃时,硝酸钾的溶解度为110g;
(3)图中点A所对应的是该温度下硝酸钾的___________(选填“饱和”或“不饱和”)溶液。
-
科目: 来源: 题型:
查看答案和解析>>【题目】水与人类的生活息息相关。
(一)、天然水净化为自来水的主要流程如下:
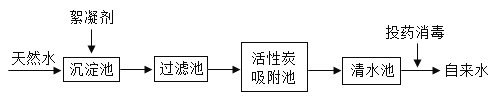
(1)下列说法不正确的是(填字母)________。
A.过滤池可以除去难溶性杂质 B.活性炭吸附池可以除去水中的色素和臭味 C.清水池中一定是软水
(2)明矾(主要成分KAl(SO4)m)能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m=______
(3)生活中,人们常用__________检验水样品是硬水还是软水。硬水危害人们健康,生活中软化硬水最常用、最简单的方法是____________。
(4)水是生命之源,我国水资源总量虽位居世界第六位,但人均水量很少。请你写出一条节约用水的方法:_____________________。
(二)、下图是实验室电解水原理的装置图
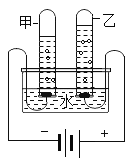
(1)保持水的化学性质的最小微粒是________,图中试管乙中的气体是______(均填名称)。
(2)电解水的化学方程式是_________________________。
(3)实验室用“电解水”或“氢气在氧气中燃烧”的实验探究水的组成元素,理论依据是______。
相关试题

