
【题目】下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
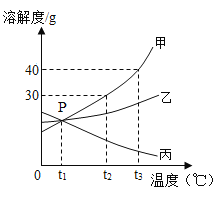
(1)P点表示在温度t1℃时,三种物质的溶解度__________。
(2)t2℃时,在温度变化的情况下要将丙的不饱和溶液变成饱和溶液的方法是___________(任写一种)。
(3)t2℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,所得溶液的质量是______g。
(4)t3℃时,三种物质的溶解度由大到小的顺序为__________。
(5)将t3℃时丙的饱和溶液降温到t2℃,溶液中溶质的质量分数________(填“变大”、“变小”或“不变”)。
【答案】相等 加入固体丙或恒温蒸发水 65 甲>乙>丙 不变
【解析】
(1)由图可知,t1℃时,甲、乙、丙的溶解度曲线相交于P点,故P点表示在温度t1℃时,三种物质的溶解度相等;
(2)由图可知,丙的溶解度随温度的升高而减小,故要将丙的不饱和溶液变成饱和溶液的方法,可采取增加丙物质、恒温蒸发溶剂或升高温度;
(3)由图可知,t2℃时,甲物质的溶解度是30g,即该温度下,100g水中最多能溶解30g甲物质,50g水最多能溶解15g甲物质,故t2℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,所得溶液的质量是:15g+50g=65g;
(4)由图可知,t3℃时,三种物质的溶解度由大到小的顺序为:甲>乙>丙;
(5)由图可知,丙的溶解度随温度的升高而减小,故将t3℃时丙的饱和溶液降温到t2℃,丙的溶解度增加,丙变为不饱和溶液,溶液的溶质质量分数不变。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:
【题目】下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是
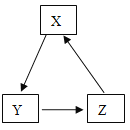
物质选项 | A | B | C | D |
X | Na2SO4 | BaCl2 | Cu | CaO |
Y | NaCl | Ba(NO3)2 | CuO | CaCl2 |
Z | NaNO3 | BaCO3 | CuSO4 | CaCO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CO2是如何被发现的?化学家又是如何研究它的性质?让我们重温这段历史。
(1)17世纪初,比利时化学家海尔蒙特研究发现,木炭燃烧后,有灰烬还有不可见的气体产生,烛火在该气体中会熄灭。另外他还在地窖、洞穴等地发现过这种气体。“烛火在该气体中会熄灭”和出现在“地窖、洞穴等地”说明这种气体具有__________的性质。
(2)1755年,英格兰化学家布莱克做了如下实验:煅烧白垩(石灰石),将煅烧生成的固体与水反应,反应后的物质与煅烧生成的气体又结合成白垩。他将这种固定在白垩中的气体叫作“固定气体”。实验②中所发生反应的化学方程式为___________。实验③中所发生反应的化学方程式为______。
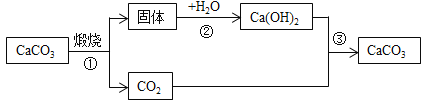
(3)1766年,英国化学家卡文迪许实验测得:一定温度下,1体积水能溶解比1体积稍多的“固定气体”。1774年,德国化学家伯格曼将石蕊溶液滴到溶有CO2的水中,石蕊溶液由紫色变成微红色。当时已经发现石蕊溶液是一种酸碱指示剂。卡文迪许和伯格曼两位化学家的实验说明CO2不仅能溶于水,还可与水反应。CO2与水反应的化学方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
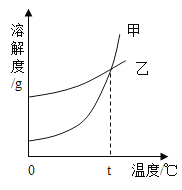
【题目】K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 20 | 40 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 117 | 121 | 126 | 139 |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
A.K2CO3的溶解度大于KNO3
B.乙代表K2CO3的溶解度曲线
C.t应在50℃~60℃之间
D.40℃时,100gKNO3饱和溶液中含63.9gKNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠俗称纯碱或苏打,在生活、生产和实验硏究中均有广泛应用。
(配制溶液)配制溶质质量分数分別为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是______(填字母)。
a.用托盘天平称取2gNa2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 | Ⅰ | Ⅱ | Ⅲ |
溶质质量分数 | 1% | 2% | 4% |
溶液pH | 11.62 | 11.76 | 11.90 |
分析I、Ⅱ、Ⅲ三组数据可得出的结论是________。
(制备物质)用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
(已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀)
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是______(填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:![]() ,则X的化学式为___________。
,则X的化学式为___________。
(标定浓度)标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于1g·mL-1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数_____(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将_____(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素有防癌和抗癌作用,如图,甲是硒的原子结构示意图,乙是硒元素在元素周期表中的信息,下列说法正确的是

A.硒原子核内中子数为34
B.硒原子在化学反应中易得到电子
C.硒元素的元素符号为Se,是一种金属元素
D.硒的相对原子质量为78.96g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数 | 加盐酸前 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀盐酸的质量(g) | 0 | 20 | 20 | 20 | 20 | 20 |
锥形瓶内物质的总质量(g) | 11.5 | 31.4 | m | 71.2 | 91.1 | 111.1 |
(查阅资料)碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,甲、乙、丙、丁、戊五种物质(或其溶液)俨然是滑冰赛道上参加接力比赛的“运动员”,相邻“运动员”之间能发生化学反应。已知:五种物质分别是 Fe、HCl、NaOH、CaCO3 和 CuCl2,中的一种,其中,甲是单质,丁与戊反应产生的气体可以熄灭终点的火炬。
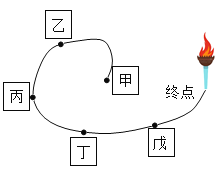
(1)甲能分别与另四种物质中的_____、_____反应(写化学式)。
(2)丁与戊反应的化学方程式为_____。
(3)丙与丁的反应属于_____(填基本反应类型)。
(4)若把无机物按单质、氧化物、酸、碱和盐进行分类,无机物 X 的类别不同于上述五种物质,如果用 X 替换戊,它也能与丁反应生成一种生活中常用的液态灭火剂,X 是________(写一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中的“碳循环”和“氧循环”为生态系统的正常运转提供了可靠的资源保障,循环过程中CO2起着非常重要的作用,如图是这种作用的具体体现之一。
![]()
(1)CO2的水溶液能使紫色石蕊试液变红色,其原因是__________(用化学方程式表示)。
(2)有机物A完全燃烧的化学方程式: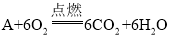 ,则A的化学式是_____________。
,则A的化学式是_____________。
(3)下列关于“碳循环”和“氧循环”的说法错误的是______(填序号,下同)。
A.无机物和有机物性质不同,但在一定条件下能相互转化
B.碳循环和氧循环分别是指二氧化碳和氧气的循环
C.绿色植物通过光合作用,将太阳能转化成化学能
D.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
(4)煤的燃烧会产生大量CO2;通过煤的综合利用可获得多种产品,有很多用途,其中焦炭广泛应用于炼铁。下列说法正确的是____。
A.煤加工成焦炭的变化属于物理变化
B.人类只能通过燃料的燃烧获取能量
C.煤燃烧产生的二氧化碳是污染空气的主要物质
D.煤是复杂的混合物,除了含有碳、氢元素外,还含有少量硫、氮等元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com