【题目】如图是学生经常使用的交通工具:自行车,请完成下列各题:
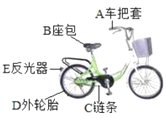
(1)由金属材料制成的有_________________ (选一种物质填序号);
(2)车轮的钢圈在潮湿的空气中会生锈,铁生锈是和空气中氧气及_______________ 发生反应,用 稀硫酸除铁锈的原理是________________(用化学方程式表示);
(3)利用铁生锈的原理在食品工业上还有应用,“纳米α-Fe 粉”,可以用于食品保鲜,称之 为“双吸剂”,请用化学方法检验使用一段时间后的“双吸剂”是否完全失效,写出鉴别过 程_________。
参考答案:
【答案】 C 水 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 取样,向其中加入足量稀盐酸,若有气泡则没有完全失效,否则已完全失效
【解析】本题考查了金属材料及其应用,金属的化学性质,金属锈蚀的条件及其防护,酸的化学性质。
(1)链条属于金属材料,车把套、座包、轮胎、反光器等物质属于合成材料;故填:C;
(2)铁在与水和氧气并存时易生锈;硫酸与氧化铁反应生成硫酸铁和水,化学方程式表示为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)若“双吸剂”完全失效则不含有铁,铁与盐酸反应生成氯化铁和氢气,可以加入盐酸鉴别,鉴别过程为取样,向其中加入足量稀盐酸,若有气泡则没有完全失效,否则已完全失效。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三种物质的溶解度曲线如右图所示,据图回答:
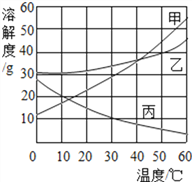
(1)30 ℃时,三种物质的溶解度由大到小的顺序为____________;
(2)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是________________;
(3)50 ℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是________,所得溶液中溶质质量分数最大的是_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产氯化钙晶体的流程如下:(原料石灰石中含的杂质主要是MgCO3、MgSO4 和Al2O3)
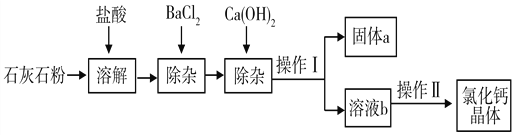
(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为_____________________;
(2)加入BaCl2是为了除去_________________;(填化学式)
(3)操作Ⅱ的具体步骤为___________________ 、冷却结晶;
(4)固体a的成分中含有的物质有_____________________(填化学式)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】煤和天然气是是当今社会重要的能源。
(1)写出天然气中甲烷完全燃烧的化学方程式_____
(2)天然气属于_____能源(填“可再生”或“不可再生”),分析下表,与煤相比,用天然气作燃料的优点有_____。
1g 物质完全燃烧
产生二氧化碳的质量/g
放出的热量/KJ
甲烷
2.75
56
碳
3.67
32
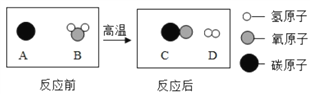
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,写出该反应化学方程式_______;
(4)液态二氧化碳可用于扑救档案室发生的火灾,下列说法不正确的是________填字母序号)。
A.液态二氧化碳汽化后不会污染档案 B.二氧化碳可覆盖在可燃物表面,隔绝空气 C.液态二氧化碳汽化时吸热,降低可燃物的着火点
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时 有较多的气泡放出,生成的是什么气体呢?同学们决定进行探究,探究前老师提示,该反应 生成的气体只有一种。
(提出猜想)放出的气体可能是 SO2、O2、H2,提出猜想的依据是__________________;
(查阅资料)SO2 易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊, 生成 CaSO3。
(方案设计)根据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是 O2,则检验方法是______________________;
(2)SO2 是一种空气污染物,容易形成酸雨,试写出酸雨的一种危害_____,乙 同学认为是 SO2,可用氢氧化钠溶液吸收,写出该反应的化学方程式________;
(3)实验小组同学合作了如下组合实验方案,排除和验证猜想的气体。
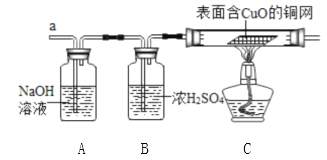
实验开始时,先将收集到的气体从 a 通入一段时间后,再点燃 B 处酒精灯,这样操作的目的是__ ,实验小组的同学在实验过程中发现 A 装置中溶液不变浑浊,B 装置中表面含 CuO 的铜网由黑色变为光亮的红色;根据现象,你 认为硫酸铜溶液中一定含有的离子是__________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示。请回答:
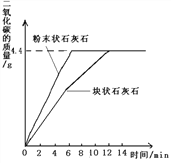
(1)由图中曲线分析得出,影响该化学反应速率的因素是:__________;
(2)每份样品充分反应后.生成二氧化碳的质量为____________.
(3)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为_____________。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确到0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置和仪器的示意图,回答下列问题。

(1)图中仪器A的名称_________;
(2)写出实验室制取二氧化碳的化学方程式_______________,要制取8.8g CO2需要_______g含碳酸钙80%的大理石;若要制取并收集较多的CO2,应选择的仪器有F、C、____(填序号);
(3)上述装置,还可用于实验室制取氧气,反应后要过滤分离出二氧化锰,除了烧杯,玻璃棒外,还需补充的玻璃仪器名称是________。
相关试题

