【题目】馒头、面包等发面食品的一个特点是面团中有许多小孔, 他们使发面食品松软可口。小明学习相关化学知识后, 将家里制作馒头用的白色粉末带到实验室与兴趣小组的同学一起进行探究。
【初步探究】取少量白色粉末于试管中, 加适量水, 测得溶液的 pH >7, 说明溶液呈 性。[来
【提出问题】白色粉末成分是什么?
【查阅资料】
(1)碳酸钠、碳酸氢钠都可用于制作发面食品。
(2)碳酸氢钠不稳定, 受热易分解生成二氧化碳和水等; 碳酸钠很稳定。
【猜想与假设】
猜想Ⅰ: 碳酸钠
猜想Ⅱ: 碳酸氢钠
【实验探究】甲乙兴趣小组设计不同实验方案进行探究。
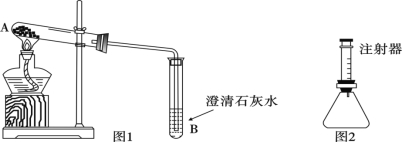
甲组方案: 如图 1, 取适量白色粉末于试管中, 将导管伸入澄清石灰水, 加热, 澄清石灰水变浑浊, 猜想Ⅱ正确。写出装置 B 中反应的化学方程式 。
乙组方案: 用如图 2 所示装置作为反应容器, 准确测量生成气体的体积以判断白色粉末的成分。
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中, 注入等体积、等浓度的足量的稀盐酸, 记录如表:
实验编号 | 锥形瓶内物质[ | 最终得到 CO2 体积 /ml | |
名称 | 质量 /g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 白色粉末 | m | V3 |
实验①的化学反应方程式为 ; 表中 m = g; 根据上表中数据分析, 猜想Ⅱ正确, 判断的依据是 。
【反思应用】
(1)甲组方案中, 无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物; 乙组方案可以判断, 如果是两者的混合物, 应该满足的条件是 。
(2)家中制作馒头、面包时, 将面粉发酵 ( 产生有机酸) , 再加入适量的碳酸氢钠, 可以使馒头、面包松软。原因是 。
参考答案:
【答案】【初步探究】碱
【实验探究】甲组方案:CO2+Ca(OH)2 ══CaCO3↓+H2O
乙组方案:Na2CO3+2HCl══2NaCl+CO2↑+H2O ; a V3=V2
【反思应用】 (1) V1<V3<V2 (2)白色粉末与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔。
【解析】【初步探究】pH<7的溶液呈酸性,pH>7的溶液呈碱性。现测得溶液的 pH >7, 说明溶液呈碱性;【实验探究】甲组方案:加热后将生成的气体通入澄清石灰水中,澄清石灰水变浑浊,说明生成了二氧化碳。二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式表示为CO2+Ca(OH)2 ══CaCO3↓+H2O;乙组方案:实验①是碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式表示为:Na2CO3+2HCl══2NaCl+CO2↑+H2O;通过测量生成气体的体积以判断白色粉末的成分,那么可取相同质量的白色粉末,通过比较生成的二氧化碳的质量来判断白色粉末是碳酸钠还是碳酸氢钠,故m=ag;猜想Ⅱ正确,说明等质量的白色粉末和碳酸氢钠产生的二氧化碳的质量一样多,即V3=V2;【反思应用】 (1)根据化学方程式可知等质量的碳酸钠和碳酸氢钠分别与足量的稀盐酸反应,碳酸氢钠产生的二氧化碳的量更多,若白色粉末是碳酸钠和碳酸氢钠的混合物,那么产生的二氧化碳在两者之间,即V1<V3<V2;(2)碳酸氢钠能与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某课外兴趣小组设计利用废旧干电池中的锌皮和未知浓度的稀盐酸制取纯净、干燥的氢气, 并验证气体中是否含有杂质。实验装置图如下:
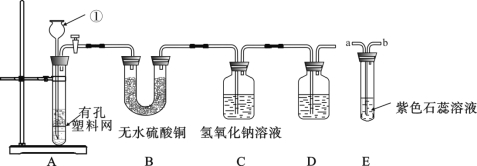
【查阅资料】无水硫酸铜遇水变蓝色
(1)装置 A 中仪器①的名称是 ; 写出发生反应的化学方程式 。
(2)实验中看到 B 中无水硫酸铜变蓝色, 说明产生的气体中含有杂质水。为了检验气体中还可能存在的杂质, 可将 E 装置连接到上述装置 ( 填序号) 之间, 气体从 (填 a 或 b) 进入装置 E 。
(3)D 装置中的试剂是 ( 写出名称) 。
(4)下列收集氢气的方法中符合题意的是 。
A.排水法 B.向下排空气法 C.干瘪的塑料袋 D.塑料瓶
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
工业上生产尿素[ CO ( NH2 ) 2 ] 的反应微观示意图如下:

(1)从微观角度看, 上图中四种物质都是由 构成。
(2)从宏观的角度看, 上图四种物质中属于氧化物的有 ( 填字母序号) 。
(3)写出工业上生产尿素的化学方程式 。
(4) 锂是一种活动性比铁强的金属, 化学式为 Li, 锂原子结构示意图为
 , 写出锂与稀硫酸反应的化学方程式 。
, 写出锂与稀硫酸反应的化学方程式 。 -
科目: 来源: 题型:
查看答案和解析>>【题目】化学与我们的生活息息相关。
(1) 包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等。其中富含糖类的是 , 不属于有机物的是 。
(2) 老年人缺 会发生骨质疏松, 容易骨折。
(3) 塑料盆、铁锅, 陶瓷茶杯等是生活常见用品, 其中属于有机合成材料的是 。
(4) 活性炭能除去家庭装修中产生的有害气体, 这是利用了活性炭的 性。
(5) 加了洗涤剂的水能除去衣服上的油污, 是利用了洗涤剂的 作用。
(6) 下列关于水的说法错误的是 ( )
A.煮沸可以将硬水转化为软水
B.工业废气直接排放会造成水污染
C.寻找合适的催化剂, 利用光照使水分解是理想的制氢方法
D.大量使用农药、化肥能提高农作物产量, 不会造成水污染
(7) 过氧化钙( CaO2 ) 能用于鱼类运输时的制氧剂, 与水反应生成碱和一种气体, 写出反应的化学方程式 。
(8) 某注射用药液的配制方法如下:
①把 1.0g 药品溶于水配制成 4.0mL 溶液 a;
②取 0.1mL 溶液 a, 加水稀释至 1.0mL, 得溶液 b;
③取 0.1mL 溶液 b, 加水稀释至 1.0mL, 得溶液 c;
④取 0.4mL 溶液 c, 加水稀释至 1.0mL, 得溶液 d。
由于在整个配制过程中药液很稀, 其密度都可近似看做 1g/cm3 , 1g 该药品可配制溶液d 的体积是 mL。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列对实验现象描述正确的是( )
A.镁在空气中燃烧发出耀眼的白光,生成氧化镁
B.硫在空气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体
C.烧杯中有两支高低不同正在燃烧的蜡烛,在蜡烛对侧沿烧杯壁缓慢倾倒二氧化碳,蜡烛由低到高依次熄灭
D.紫色的石蕊溶液滴到白醋中,石蕊溶液变蓝
-
科目: 来源: 题型:
查看答案和解析>>【题目】对下列宏观事实的微观解释,不合理的是( )
A.车胎在阳光下爆裂——分子体积变大
B.氧化汞受热后分解——分子在化学变化中可分
C.闻到不远处的花香——分子在不断地运动
-
科目: 来源: 题型:
查看答案和解析>>【题目】生活中处处充满化学,下列说法正确的是( )
A.甲醛可用来保鲜食品 B.“地沟油”可烹调食品
C.补铁可预防骨质疏松 D.吃蔬菜可补充维生素
相关试题

