【题目】日常生活中所说的盐,通常指食盐(主要成分是氯化钠)。
(1) 通过晾晒海水,可以蒸发除去水分,得到粗盐。通常不采用降低海水温度的方法得到粗盐,是因为_____________,相同情况下降温析出的晶体比较少。
(2)根据“粗盐中难溶性杂质的去除”实验,回答有关问题。
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.1g。
②过滤
③蒸发 在加热过程中,用玻璃棒不断搅拌,防止_______。当蒸发皿中___,停止加热。
④计算产率 得到精盐3.3g,则精盐的产率为__________(计算结果保留一位小数)。
(3)若经过上述实验得到的精盐中还含有氯化镁、氯化钙,为了除去这两种可溶性杂质,可将得到的精盐全部溶于水,加入过量的氢氧化钠溶液和__________溶液,充分反应后,接下来的操作顺序是__________(填序号)。
①蒸发 ②加入过量的稀盐酸 ③过滤
参考答案:
【答案】氯化钠的溶解度受温度变化影响很小 局部温度过高,造成液滴飞溅 出现较多量固体 84.6% 碳酸钠溶液 ③②①
【解析】
(1)氯化钠是由Na+、Cl-构成的;
(2)通常不采用降低海水温度的方法得到粗盐,是因为氯化钠的溶解度受温度变化影响较小,相同情况下降温析出的晶体比较少;
(3)在加热过程中,用玻璃棒不断搅拌,防止液体外溅,当蒸发皿中出现较多固体时,停止加热;
④精盐的产率为:![]() ×100%≈84.6%;
×100%≈84.6%;
(4)为了除去这两种可溶性杂质,可将得到的精盐全部溶于水,加入过量的氢氧化钠溶液和碳酸钠溶液,以除去氯化镁、氯化钙,充分反应后,接下来的操作顺序是过滤、加入过量的稀盐酸、蒸发。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙、丁四种物质的相互反应关系如图所示,“—”表示相连的物质间能发生反应,下列符合对应反应关系的选项是

选项
A
B
C
D
物
质
甲
Ca(OH)2
CO2
H2
Mg
乙
Na2CO3
NaOH
O2
HCl
丙
H2SO4
CaCl2
CuO
CuSO4
丁
BaCl2
K2CO3
HCl
NaOH
A. AB. BC. CD. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】“如图”表示元素的化合价与物质类别关系。若它表示氮元素的部分关系图。则:
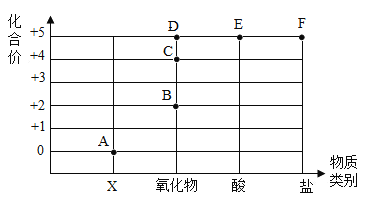
(1) A点对应的物质类别是______;
(2)写出B点、E点表示物质的化学式各一个为 _________ 、_______ 。
(3)某化合物的化学式为KNO3,它代表的点是______(填字母);
(4)根据物质的_____________,可以把物质分成混合物和纯净物。
(5)完成鉴别氯化钾和氯化铵两种固体化肥的实验报告。
实验步骤
实验现象
实验结论
_________
_________
_________
-
科目: 来源: 题型:
查看答案和解析>>【题目】防治污染,保护环境,实现可持续发展。
(1)下列属于空气污染物的是_________。
A.臭氧 B.一氧化碳 C.PM2.5 D.PM10
(2)① 化石燃料是________(填“可再生能源”或“不可再生能源”),它们燃烧会造成空气污染,应合理利用与开发。
②下列防治水体污染的措施正确的是______。
A.禁止使用农药和化肥 B.生活污水集中处理、达标排放
C.工业废水处理后达标排放 D.将废旧电池深埋地下
(3)甲、乙两个城市全年雨水的月平均pH变化 如图。
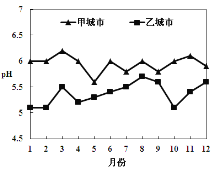
下列说法正确的是________。
A.甲城市受酸雨的影响较严重
B.pH小于7的降雨称为酸雨
C.煤的大量燃烧是造成酸雨的主要原因之一
D.大力推广使用脱硫煤可以减少酸雨的形成
-
科目: 来源: 题型:
查看答案和解析>>【题目】水与人们的生活有着密切的关系。

(1)为验证水的组成用如右图所示装置进行实验。
①写出该反应的化学方程式___________________。
②电解水的过程中,发生改变的微粒是_______(写名称)。
③下列物质溶于水后能导电的是______(填字母)。
A.蔗糖 B.氯化氢 C.氯化钠 D.氢氧化钙
(2)配制200g质量分数为5%的氢氧化钠溶液,需要需要水____mL。配制时用到玻璃仪器有________、烧杯、玻璃棒和胶头滴管。(水的密度近似看作1g/cm3)
(3)用配得氢氧化钠溶液与某硫酸溶液反应,下图是利用数字化传感器得到的溶液pH变化图像。
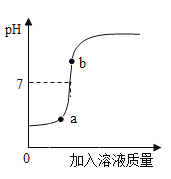
①根据图中曲线,判断进行的操作是______(填字母)。
A.将硫酸溶液逐滴滴加到氢氧化钠溶液中
B.将氢氧化钠溶液逐滴滴加到硫酸溶液中
②从微观角度分析,该反应实质为___________ 。
③b点对应的溶液中的溶质为____________写化学式)。
④若80g 5%的氢氧化钠溶液能恰好中和50g硫酸溶液,试计算该硫酸溶液的溶质质量分数_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是a、b两种固体物质(不含结晶水)的溶解度曲线。下列说法正确的是
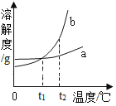
A. t1℃时,a、b两物质溶解度相等
B. 将t2℃时b溶液降温至t1℃,一定有固体析出
C. 若b中混有少量的a,可用蒸发结晶的方法提纯b
D. t2℃时,b溶液的溶质质量分数一定大于a溶液的溶质质量分数
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列四个图像分别对应四个变化过程,其中不正确的是
A.
 电解水
电解水B.
 向一定量的氢氧化钡溶液中不断加入稀硫酸
向一定量的氢氧化钡溶液中不断加入稀硫酸C.
 向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸
向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸D.
 表示向一定量的氢氧化钠和碳酸钠的混合溶液中,逐滴加入过量的稀盐酸溶液
表示向一定量的氢氧化钠和碳酸钠的混合溶液中,逐滴加入过量的稀盐酸溶液
相关试题

