【题目】甲、乙、丙、丁四种物质的相互反应关系如图所示,“—”表示相连的物质间能发生反应,下列符合对应反应关系的选项是

选项 | A | B | C | D | |
物 质 | 甲 | Ca(OH)2 | CO2 | H2 | Mg |
乙 | Na2CO3 | NaOH | O2 | HCl | |
丙 | H2SO4 | CaCl2 | CuO | CuSO4 | |
丁 | BaCl2 | K2CO3 | HCl | NaOH | |
A. AB. BC. CD. D
参考答案:
【答案】A
【解析】
A、氢氧化钙会与碳酸钠、稀硫酸反应,碳酸钠会与氢氧化钙、稀硫酸、氯化钡反应,硫酸会与碳酸钠、氢氧化钙、氯化钡反应,氯化钡会与硫酸、碳酸钠反应,故A正确;
B、弱酸不会换出强酸,二氧化碳与水反应生成碳酸,所以二氧化碳不会与氯化钙反应,故B错误;
C、氧气、金属氧化物都具有氧化性,所以氧气不会与金属氧化物,故C错误;
D、硫酸盐只有硫酸钡难溶于水,氯化铜溶于水,盐酸会与硫酸铜交换成分不会生成沉淀、气体、水不符合复分解反应的条件,故D错误。
故选A。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置图,回答有关问题:

(1)写出有标号的仪器名称:a ,b .
(2)实验室选用A、F装置制取氧气,化学方程式为 .
(3)实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为 ,若要得到平稳的气流,应选择的发生装置是 (填字母),选用D装置收集二氧化碳的原因是 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO2通入NaOH溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验
序号
实验步骤一
实验步骤二
实验
序号
实验步骤一
实验步骤二
实验I


实验II

(探究与结论)
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是____________________。(2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程式是__________。
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是____________________。
(拓展延伸)现有下列信息:
资料卡片一
20℃NaOH、Na2CO3在水中的溶解度
物质 溶解度(S)/g
NaOH 109
Na2CO3 21.8
资料卡片二
20℃NaOH、Na2CO3在乙醇中的溶解度
物质 溶解度(S)/g
NaOH 17.3
Na2CO3 <0.01
请你和化学兴趣小组的同学一起利用以上料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:_____________________________。
看到的现象是_________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~E均为初中化学常见的物质,它们之间的关系如图所示(部分物质已经略去)。已知A是目前世界上年产量最高的金属;B是胃酸的主要成分;C中金属元素的质量分数为40%, 其水溶液呈蓝色,常用来配制农药波尔多液;D属于碱;E属于盐。则C的化学式为__________;A与B反应的化学方程式为__________;E转化为D的化学方程式为__________。
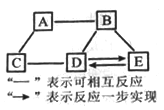
-
科目: 来源: 题型:
查看答案和解析>>【题目】“如图”表示元素的化合价与物质类别关系。若它表示氮元素的部分关系图。则:
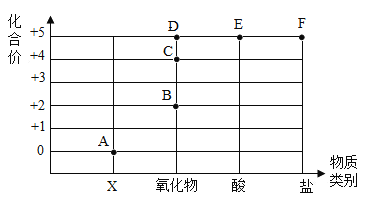
(1) A点对应的物质类别是______;
(2)写出B点、E点表示物质的化学式各一个为 _________ 、_______ 。
(3)某化合物的化学式为KNO3,它代表的点是______(填字母);
(4)根据物质的_____________,可以把物质分成混合物和纯净物。
(5)完成鉴别氯化钾和氯化铵两种固体化肥的实验报告。
实验步骤
实验现象
实验结论
_________
_________
_________
-
科目: 来源: 题型:
查看答案和解析>>【题目】防治污染,保护环境,实现可持续发展。
(1)下列属于空气污染物的是_________。
A.臭氧 B.一氧化碳 C.PM2.5 D.PM10
(2)① 化石燃料是________(填“可再生能源”或“不可再生能源”),它们燃烧会造成空气污染,应合理利用与开发。
②下列防治水体污染的措施正确的是______。
A.禁止使用农药和化肥 B.生活污水集中处理、达标排放
C.工业废水处理后达标排放 D.将废旧电池深埋地下
(3)甲、乙两个城市全年雨水的月平均pH变化 如图。
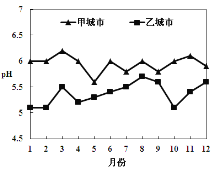
下列说法正确的是________。
A.甲城市受酸雨的影响较严重
B.pH小于7的降雨称为酸雨
C.煤的大量燃烧是造成酸雨的主要原因之一
D.大力推广使用脱硫煤可以减少酸雨的形成
-
科目: 来源: 题型:
查看答案和解析>>【题目】日常生活中所说的盐,通常指食盐(主要成分是氯化钠)。
(1) 通过晾晒海水,可以蒸发除去水分,得到粗盐。通常不采用降低海水温度的方法得到粗盐,是因为_____________,相同情况下降温析出的晶体比较少。
(2)根据“粗盐中难溶性杂质的去除”实验,回答有关问题。
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.1g。
②过滤
③蒸发 在加热过程中,用玻璃棒不断搅拌,防止_______。当蒸发皿中___,停止加热。
④计算产率 得到精盐3.3g,则精盐的产率为__________(计算结果保留一位小数)。
(3)若经过上述实验得到的精盐中还含有氯化镁、氯化钙,为了除去这两种可溶性杂质,可将得到的精盐全部溶于水,加入过量的氢氧化钠溶液和__________溶液,充分反应后,接下来的操作顺序是__________(填序号)。
①蒸发 ②加入过量的稀盐酸 ③过滤
相关试题

