【题目】已知某金属X有下列相关信息:① 它的主要矿物的化学成分是X2O3;② 它主要通过热还原法冶炼而成;③ 它的年产量位于金属之首。
(1) 据此推断X是_____________(填选项字母)。 A.钛 B.铁 C.铝 D.铜
(2)在高炉中用含X2O3的矿物冶炼该金属的原理是____________(用化学方程式表示)。
(3)同学们设计了如下实验方案测定该矿物中X2O3的质量分数(装置气密性良好;矿物中的杂质不参加反应;假设矿物样品中的X2O3完全反应):
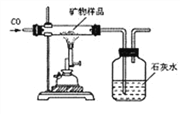
①取矿物样品并称量该样品的质量;
②测出反应前广口瓶和瓶内物质总质量;
③测出反应后广口瓶和瓶内物质总质量; ④计算得出矿物样品中x2O3的质量分数。
a. 你认为,该实验方案___________(填“一定”或“不一定”)能准确测出矿物中X2O3的质量分数,理由是____________________________ .
b. 不改变装置和药品,你还可以通过测定哪些数据,再通过计算得出矿物中X2O3的质量分数:_________________________________。
c. 从环保角度看,该装置的不足之处是____________________。
参考答案:
【答案】 B X2O3+3CO 高温 2X+3CO2(或Fe2O3+3CO高温 2Fe+3CO2) a不一定 生成的二氧化碳气体不一定被石灰水完全吸收(或石灰水可能吸收空气中的二氧化碳) 分别测出反应前玻璃管和矿物样品的总质量、反应后玻璃管和剩余固体总质量(或测出反应后玻璃管内剩余固体的质量) 无尾气处理装置
【解析】(1) 据此推断X是B.铁,它的年产量位于金属之首。(2)在高炉中用含X2O3的矿物冶炼该金属的原理是∶X2O3+3CO![]() 2X+3CO2(或Fe2O3+3CO
2X+3CO2(或Fe2O3+3CO![]() 2Fe+3CO2)。(3) 测定该矿物中X2O3的质量分数。a. 该实验方案不一定能准确测出矿物中X2O3的质量分数,理由是生成的二氧化碳气体不一定被石灰水完全吸收(或石灰水可能吸收空气中的二氧化碳)。b. 不改变装置和药品,还可以通过测定反应前玻璃管和矿物样品的总质量、反应后玻璃管和剩余固体总质量(或测出反应后玻璃管内剩余固体的质量),再通过计算得出矿物中X2O3的质量分数。c. 从环保角度看,该装置的不足之处是无尾气处理装置,尾气污染环境。
2Fe+3CO2)。(3) 测定该矿物中X2O3的质量分数。a. 该实验方案不一定能准确测出矿物中X2O3的质量分数,理由是生成的二氧化碳气体不一定被石灰水完全吸收(或石灰水可能吸收空气中的二氧化碳)。b. 不改变装置和药品,还可以通过测定反应前玻璃管和矿物样品的总质量、反应后玻璃管和剩余固体总质量(或测出反应后玻璃管内剩余固体的质量),再通过计算得出矿物中X2O3的质量分数。c. 从环保角度看,该装置的不足之处是无尾气处理装置,尾气污染环境。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明和小英要验证一块石头是否含碳酸钙。
(1)小明说:“只要取一小块石头放在烧杯中,再在石块上倒入盐酸,发现有大量气泡产生,就能证明石块含有碳酸钙。”小英说:“在石块上倒盐酸,产生的大量气泡是盐酸挥发而成的。”小英的说法对吗?_______(填“对”或“不对”)。
(2)小明和小英带着问题请教王老师,在王老师的指导下,进行了下列实验探究,其实验过程如下:①取一小块石块置于烧杯中,滴加盐酸后,发现产生了无色无味气体;②在老师的指导下,取①中的溶液检验,石块中含有钙元素;③他们又设计了如图所示的实验装置,在实验中观察到广口瓶中有浑浊现象产生。
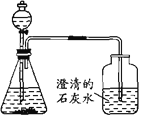
在上述实验中,他们进行的是_______实验研究(填“定性”或“定量”)。
(3)假若称取10.0 g石块与足量的稀盐酸反应(杂质不与盐酸反应),并用饱和石灰水吸收,得到的沉淀经适当处理后得干燥固体7.5 g。计算:
①石块中含碳酸钙的质量分数_______________;
②已知CO2在标准状况下的密度为1.98 g/L,则生成标准状况下CO2气体的体积为______________毫升?
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属材料在生活、生产中应用十分广泛。

(1)图A是金属的一个应用实例,请说出这利用了金属的什么物理性质(答出一点即可)?______________________________
(2)图B是两块金属片相互刻划后,在纯铜片上有明显的划痕。该实验探究的目的是什么?________________________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
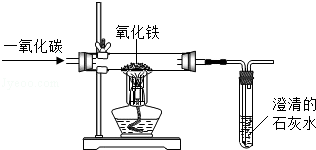
A.实验时,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成
B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁
C.反应后,玻璃管中的固体物质的质量比反应前减少了,证明一定有铁生成
D.为了减少空气污染,应增加尾气处理装置
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业明胶是用工业皮革废料,经生石灰浸渍膨胀等序制成的“蓝皮胶”,被不法商人添加到食品、药物中,变成“毒食”、“毒胶囊”。经检测,“毒食”和“毒胶囊”中铬超标数十倍,食用后对肝、肾会造成极大伤害,导致癌症。
⑴上述中的“铬”是指________(填序号)。
A.单质 B.原子 C.元素 D.分子
⑵下图是元素周期表中的一格,从图中获得的信息正确的是________。
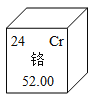
A.该元素的质子数是52 B.该元素在地壳中的含量为24%
C.该元素属于非金属元素 D.该元素的一个原子核中含有28个中子
⑶ 交警常用装有重铬酸钾的仪器检测司机是否酒后驾车,因为酒精可以使橙红色的重铬酸钾变为绿色的硫酸铬,硫酸铬[Cr2(SO4)3]中铬元素的化合价为________ 价。
-
科目: 来源: 题型:
查看答案和解析>>【题目】颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”。请回答以下问题:
(1) 写出生成“纳米铁”的化学方程式____________________________________。
(2) 反应中需要保护气的原因是__________________________________________。
(3) 某化学探究小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如下实验方案:
① 将大小一样的铁片和镁片分别加入到溶质质量分数相同的稀盐酸中;
② 将铜片加入到硝酸汞溶液中,铜片上出现银白色物质;
③ 将金属片A加入到溶液B中。
a.根据实验①判断出镁的金属活动性比铁强,依据的现象是 _____________________;
b.根据实验②的现象得出的结论是___________________________;
c.要通过实验③得出铁和铜的金属活动性顺序,那么,如果B是硫酸铜溶液,则金属A是______________,如果A是铜,则溶液B是_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某课外活动小组为测定铜锌合金粉末中铜的质量分数设计了下列实验:
①称取ag样品放入烧杯,滴入足量稀盐酸。②取一张质量为bg的滤纸,制作并安装好过滤器。③待①中反应充分后,过滤。④取沉淀连同滤纸放在干燥器中干燥后,称量,质量为cg。
回答下列问题:
(1)称量样品时,应把样品放在托盘天平的 盘里。
(2)如何判断①中反应已进行充分? 。
(3)过滤中发现滤液出现浑浊,应如何处理? 。
(4)整个实验过程中用到的玻璃仪器有烧杯、胶头滴管、 、玻璃棒、干燥器等。
(5)通过上述实验测得的铜的质量分数是 (用a、b、c表示)。
(6)老师指出,③、④之间缺少一个步骤,使得实验结果偏大。该步骤是 。
相关试题

